C6h5ona ra C6h5oh | C6H5ONa + CO2 + H2O → C6H5OH + NaHCO3

C6H5ONa ra C6H5OH là một quá trình hóa học quan trọng trong tổng hợp hữu cơ. Việc chuyển đổi từ chất C6H5ONa sang C6H5OH thường được gọi là quá trình hydrolysis. Trong quá trình này, chất C6H5ONa phản ứng với nước để tạo thành C6H5OH và NaOH. Quá trình này được sử dụng rộng rãi trong công nghiệp và trong các phản ứng hóa học để tạo ra các hợp chất hữu cơ có giá trị.
Lý thuyết về C6H5ONa ra C6H5OH
Phương trình phản ứng C6H5ONa ra C6H5OH
C6H5ONa + CO2 + H2O → C6H5OH + NaHCO3
Điều kiện phản C6H5ONa ra C6H5OH
Nhiệt độ: nhiệt độ Áp suất: cao Xúc tác: NaOH đặc
Hiện tượng nhận biết
Phương trình không có hiện tượng nhận biết đặc biệt.
Trong trường hợp này, bạn chỉ thường phải quan sát chất sản phẩm C6H5OH (Phenol) (trạng thái: lỏng) (màu sắc: không màu), NaHCO3 (natri hidrocacbonat) (trạng thái: rắn) (màu sắc: trắng), được sinh ra
Hoặc bạn phải quan sát chất tham gia C6H5ONa (Natri Phenolat) (trạng thái: dung dịch) (màu sắc: không màu), H2O (nước) (trạng thái: lỏng) (màu sắc: không màu), CO2 (Cacbon dioxit) (trạng thái: khí) (màu sắc: không màu), biến mất.
Nội dung mở rộng C6H5OH
Phenol là gì? Phân loại như thế nào?
Khái niệm về phenol:
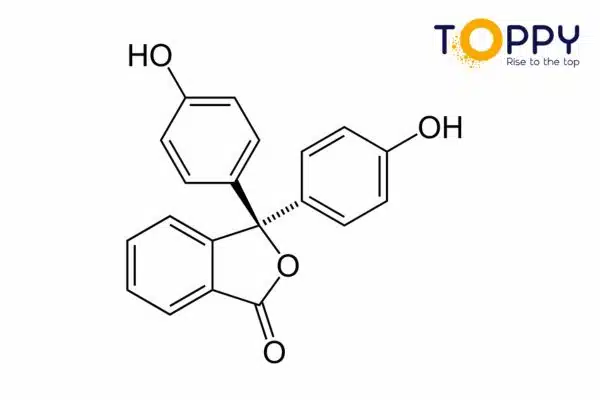
Phenol là một hợp chất hữu cơ thơm có công thứ hóa học là C6H5OH. Mỗi phân tử gồm một nhóm phenyl ( −C6H5) liên kết với một nhóm hydroxyl (-OH). Đây là một hóa chất có tính độc tố cao, cấm sử dụng trong thực phẩm, có thể gây bỏng nếu tiếp xúc với da. Hợp chất hữu cơ này có tính axit vì thế cần lưu ý khi sử dụng vì nếu để rơi vào da có thể gây bỏng.
Phân loại phenol:
- Loại monophenol: Đây là những phenol mà phân tử có chứa 1 nhóm -OH”>OH. Ví dụ: phenol, o-crezol, m-crezol, p-crezol…
- Loại poliphenol: Là những phenol mà phân tử có chứa nhiều nhóm OH”>OH.
Phenol là gì?
Những đặc điểm tính chất của phenol
Tính chất vật lý của phenol
- Phenol là một chất rắn, chúng có dạng tinh thể không màu, mùi đặc trưng và nóng chảy ở 43°C.
- Khi để lâu ở ngoài không khí, chúng sẽ bị oxy hóa một phần nên có màu hồng và bị chảy rữa do hấp thụ hơi nước.
- Ít tan trong nước lạnh và có tan trong một số hợp chất hữu cơ.
- Là chất tan vô hạn ở nhiệt độ trên khoảng 66oC.
Tính chất hóa học của phenol
Tính chất của nhóm -OH
- Tác dụng với kim loại kiềm:
C6H5OH + Na → C6H5ONa + 1/2H2
- Tác dụng với bazo mạnh tạo muối phenolate:
C6H5OH + NaOH → C6H5ONa + H2O
Tính chất của nhân thơm – Phản ứng thế H ở vòng benzen
- Thế Brom: Phenol tác dụng với dung dịch brom tạo 2,4,6 – tribromphenol kết tủa trắng:
Phản ứng này dùng để nhận biết phenol khi không có mặt của anilin. Phenol tham gia phản ứng thế brom dễ hơn benzen do có nhóm OH đẩy e làm tăng mật độ electron trong vòng benzen.
- Thế Nitro: Phenol tác dụng với HNO3 đặc có xúc tác H2SO4 đặc, nóng tạo 2,4,6 – trinitrophenol (axit picric):
C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3H2O
Phản ứng tạo nhựa phenolfomandehit
Phenol + HCHO trong môi trường axit tạo sản phẩm là nhựa phenolfomandehit.
nC6H5OH + nHCHO → nH2O + (HOC6H2CH2)n
Những đặc điểm tính chất của phenol
Điều chế Phenol ra sao?
Từ xa xưa, phenol được điều chế từ nhựa than đá. Thế nhưng hiện nay, chúng được sản xuất trên quy mô lớn (khoảng 7 tỷ kg/năm) từ các nguyên liệu có nguồn gốc từ dầu mỏ.
- Nguồn phenol chủ yếu lấy từ sản phẩm chưng cất than đá.
- Ngoài ra có thể điều chế từ benzen:
C6H6 + Br2 -> C6H5Br+ HBr (xúc tác bột Fe)
C6H5Br + 2NaOH (đặc) -> C6H5ONa + NaBr + H2O (nhiệt độ và áp suất cao)
C6H5ONa + CO2 + H2O -> C6H5OH + NaHCO3
Những ứng dụng của phenol trong cuộc sống
Phenol được ứng dụng rộng rãi trong nhiều lĩnh vực khác nhau của cuộc sống, cụ thể như sau:
- Trong công nghiệp sản xuất chất dẻo, Phenol là nguyên liệu chính để sản xuất nhựa phenol formaldehyde.
- Trong ngành công nghiệp tơ hóa học, người ta sử dụng phenol để tổng hợp ra tơ polyamide.
- Phenol được dùng để điều chế chất kích thích sinh trưởng thực vật, kích thích tố thực vật 2,4 – D, điều chế chất diệt cỏ.
- Nhờ tính diệt khuẩn cao mà phenol được sử dụng để là chất sát trùng, và điều chế thuốc diệt sâu bọ, nấm mốc.
- C6H5OH cũng là nguyên liệu chính để điều chế thuốc nổ, một số sản phẩm nhuộm.
Những ứng dụng của phenol trong cuộc sống
Phenol có độc hại hay không?
Nhiều người vẫn thắc mắc, liệu rằng phenol có phải là một chất độc hại? Thì câu trả lời ở đây là có. Phenol là một hóa chất có độc tính cao, có thể gây bỏng nặng nếu rơi vào da.
C6H5OH và các dẫn xuất của chúng đều là các chất độc gây nguy hiểm cho sức khỏe con người cũng như mọi sinh vật sống. Nó có khả năng tích lũy trong cơ thể sinh vật và gây nhiễm độc cấp tính cho con người. Nếu phenol xâm nhập vào cơ thể, chúng sẽ gây tổn thương cho các cơ quan bên trong, chủ yếu là tác động lên hệ tim mạch, hệ thần kinh và máu.
Nó còn là một chất gây ô nhiễm môi trường.
Liều lượng gây nguy hiểm cho cơ thể là 2-5 gam, trên 10gam có thể gây chết người.
Phenol là một hóa chất có độc tính cao, có thể gây bỏng nặng nếu rơi vào da
Triệu chứng khi bị ngộ độc Phenol cần biết
- Gây rối loạn tiêu hoá: nôn mửa, buồn nôn, ỉa chảy
- Rối loạn thần kinh và toàn thân: mệt mỏi, chóng mặt, nhức đầu, gầy sút nhanh
- Giãy giụa, co giật, hôn mê
- Rối loạn tuần hoàn và hô hấp, sốc nặng
- Khi tiếp xúc với dung dịch đặc có thể gây hoại tử hoặc hoại thư hoặc có thể gây tử vong ngay lập tức.
Triệu chứng ban đầu của nhiệm độc phenol là nôn mửa, tiêu chảy,…
Những lưu ý khi sử dụng phenol
Do phnol là một hóa chất vô cùng độc hại nên cần hết sức lưu ý khi sử dụng để tránh gặp phải những tác hại không mong muốn như sau:
- Không để chúng tiếp xúc trực tiếp với cơ thể, khi sử dụng cần có các biện pháp bảo hộ cần thiết theo quy định.
- Không hít hoặc nuốt phải phenol.
- Nếu như chúng dính vào mắt hoặc da thì phải rửa mắt ngay với nhiều nước ít nhất trong 15 phút và ngay lập tức tới các cơ sở y tế để được kiểm tra chuẩn xác nhất.
Những lưu ý khi sử dụng phenol
Bài tập vận dụng liên quan C6H5ONa ra C6H5OH
Câu 1: Khi cho phenol tác dụng với dung dịch brom dư thì thu được một dẫn xuất của phenol là 2,4,6-tribromphenol, trong môi trường này 2,4,6-tribromphenol là chất:
- lỏng, nhẹ hơn phenol
- lỏng, nặng hơn phenol
- rắn
- rắn, rồi tan trong phenol dư
Đáp án C
Câu 2: Benzen không phản ứng với dung dịch brom nhưng phenol làm mất màu nâu đỏ của dung dịch brom nhanh chóng vì lí do nào sau đây?
- Phenol có tính axit
- Tính axit của phenol yếu hơn cả axit cacbonic
- Phenol là dung môi hữu cơ phân cực hơn benzen
- Do ảnh hưởng của nhóm -OH, cả vị trí ortho và para trong phenol trở nên giàu điện tích âm, tạo điều kiện cho tác nhân Br− nhanh chóng tấn công
Đáp án D
Câu 3. CTPT C7H8O có số đồng phân hình học là hợp chất thơm là:
- 2
- 3
- 4
- 5
Đáp án D
Câu 4. Cho các chất: Phenol, Striren, Ancol benzylic. Thuốc thử duy nhất có thể phân biệt được ba chất lỏng đựng trong ba lọ mất nhãn là:
- Na
- Dung dịch Brom
- Dung dịch NaOH
- Quỳ tím
Đáp án B
Câu 5. Hợp chất Y là dẫn xuất chứa oxi của benzen, khối lượng phân tử của Y bằng 94 đvC. Cho biết CTCT của Y
- Ancol benzylic
- Phenol
- p-Crezol
- Natriphenolat
Đáp án B
Câu 6. Cho các phát biểu sau về phenol:
(a) C6H5OH vừa tác dụng được với dung dịch NaOH vừa tác dụng được với Na.
(b) C6H5OH tan được trong dung dịch KOH.
(c) Nhiệt độ nóng chảy của C6H5OH lớn hơn nhiệt độ nóng chảy của ancol etylic.
(d) C6H5OH phản ứng được với dung dịch KHCO3 tạo CO2.
(e) C6H5OH là một ancol thơm.
Trong các trường hợp trên, các phát biểu đúng là
- (a); (b); (c)
- (a); (c); (e)
- (a); (b); (c); (d)
- (a); (b); (d); (e)
Đáp án A
(a) C6H5OH vừa tác dụng được với dung dịch NaOH vừa tác dụng được với Na.
(b) C6H5OH tan được trong dung dịch KOH.
(c) Nhiệt độ nóng chảy của C6H5OH lớn hơn nhiệt độ nóng chảy của ancol etylic.
Câu 7. Đốt cháy hoàn toàn a gam C2H5OH thu được 0,1 mol CO2.
Đốt cháy hoàn toàn b gam CH3COOH thu được 0,1 mol CO2. Cho a gam C2H5OH tác dụng với b gam CH3COOH có xúc tác là H2SO4 đặc và đun nóng (giả sử hiệu suất phản ứng là 100%) thì thu được số gam ete là
- 8,8 gam .
- 17,6 gam
- 4,4 gam.
- 13,2 gam.
Đáp án C
Ta có
nC2H5OH = 1/2 nCO2 = 0,05 mol; nCH3COOH = 0,05 mol
Phương trình phản ứng hóa học
CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O
meste = 0,05.88 = 4,4 (gam)
Câu 8. Đun nóng a gam ancol no, đơn chức, mạch hở A với H2SO4 đặc ở nhiệt độ thích hợp thu được b gam chất hữu cơ B.
Tỉ khối hơi của B so với A bằng 0,7. Hiệu suất của phản ứng đạt 100%. A có công thức phân tử là:
- C2H5OH
- C3H7OH
- C5H11OH
- C4H9OH
Đáp án B
Ta có theo đề bài tỉ khối hơi của B so với A bằng 0,7
dB/ dA = 0,7 => X là anken
Gọi X: CnH2n+2O => Y: CnH2n
Ta có: 14n/(14n+18) = 0,7 => n = 3
Công thức phân tử: C3H7OH
Câu 9. Phản ứng tạo kết tủa trắng của phenol với dung dịch Br2 chứng tỏ rằng
- Phenol có nguyên tử hiđro linh động.
- Phenol có tính axit vì có nhóm -COOH
- ảnh hưởng của nhóm –OH đến gốc –C6H5 trong phân tử phenol
- ảnh hưởng của gốc –C6H5 đến nhóm –OH trong phân tử phenol
Đáp án C
………………………………
Quá trình hóa học C6H5ONa ra C6H5OH là một phản ứng quan trọng trong lĩnh vực tổng hợp hữu cơ. Việc chuyển đổi này tạo ra một loạt sản phẩm có giá trị, được ứng dụng trong công nghiệp và nghiên cứu khoa học. C6H5ONa là muối của axit phenol và NaOH, thông qua quá trình hydrolysis, nó chuyển đổi thành C6H5OH (phenol), NaOH. Sự chuyển đổi này tạo điều kiện thuận lợi để tổng hợp các hợp chất hữu cơ quan trọng khác, đóng góp tích cực cho sự phát triển và ứng dụng của hóa học hiện đại.
Xem thêm: