Trong hướng dẫn từ Toppy bạn đọc sẽ được tìm hiểu cách viết và cân bằng chính xác phản ứng ZnS tác dụng với dung dịch H2SO4, tạo thành ZnSO4 và H2S. Ngoài ra, cũng sẽ đưa ra những câu hỏi lý thuyết liên quan để làm rõ về quá trình phản ứng này. Mời các bạn tham khảo nội dung chi tiết dưới đây để tìm hiểu thêm về phản ứng ZnS ra H2S.
Lý thuyết về ZnS ra H2S
Phương trình phản ứng ZnS ra H2S
ZnS + H2SO4 → ZnSO4 + H2S
Điều kiện xảy ra phản ứng hóa học ZnS tác dụng H2SO4
Nhiệt độ thường
Nội dung mở rộng ZnS ra H2S
Zinc sulfide (Kẽm sulfua) là gì?
Zinc sulfide hay Kẽm sunfua là hợp chất hóa học tồn tại dưới dạng khan và dạng ngậm nước với công thức hóa học là ZnS. Đây là dạng chính của kẽm trong tự nhiên có trong khoáng vật phổ biến là sphalerit. Khoáng vật này ở dạng tinh khiết có màu trắng, tuy nhiên nó thường có màu đen do lẫn nhiều tạp chất và được sử dụng rộng rãi để làm chất tạo màu. Ở dạng tổng hợp kết chặt, kẽm sulfua có thể trong suốt và được dùng làm cửa sổ trong kính ánh sáng khả kiến hay kính hồng ngoại.
Zinc sulfide (Kẽm sulfua) là gì?
Những tính chất lý hóa của Zinc sulfide
Tính chất vật lí của Zinc sulfide
- Kẽm sulfua là chất rắn màu trắng, không mùi và tan được trong nước, dễ hút ẩm nhưng không cháy.
- Khối lượng mol: 97.474 g/mol.
- Khối lượng riêng: 4.090 g/cm3
- Điểm nóng chảy: 1.185 °C.
- Độ hòa tan trong nước: 57.7 g/100 ml.
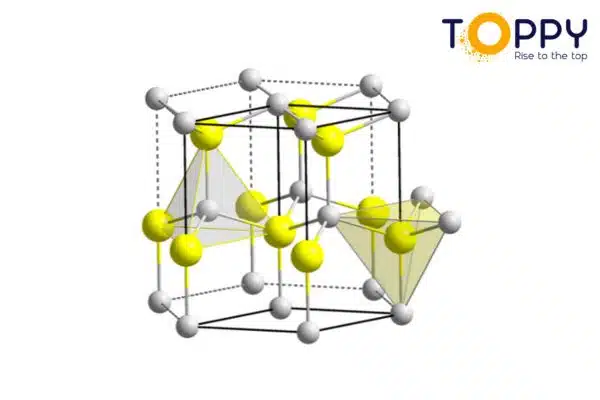
Cấu trúc tinh thể của Zinc sulfide
Tính chất hóa học của Zinc sulfide
- Zinc sulfide tác dụng với dung dịch axít tạo thành khí bay lên và muối:
2HCl + ZnS → H2S + ZnCl2
- Tác dụng với muối tạo thành hai muối mới:
ZnS + 2NaCl → ZnCl2 + Na2S
Điều chế/Sản xuất Zinc sulfide như thế nào?
Sản xuất Zinc sulfide trong công nghiệp
Zinc sulfide thường được sản xuất từ vật liệu thải của các quá trình sản xuất khác. Phổ biến từ các lò luyện nóng chảy, xỉ, và rượu lên men.
Đây cũng là một sản phẩm phụ của quá trình tổng hợp amoniac từ metan do kẽm oxit được sử dụng để hút các tạp chất hydro sunfua trong khí thiên nhiên:
ZnO + H2S → ZnS + H2O
Điều chế Zinc sulfide trong phòng thí nghiệm
Được tạo ra khi đốt cháy hỗn hợp kẽm và lưu huỳnh. Vì kẽm sunfua không tan trong nước, nên nó cũng có thể được tạo ra từ phản ứng kết tủa. Các dung dịch chứa muối Zn2+ dễ dàng tạo kết tủa ZnS khi có mặt ion sunfua (như từ H2S).
Zn2+ + S2− → ZnS
Những ứng dụng của Zinc sulfide trong đời sống
Zinc sulfide được sử dụng phổ biến trong đời sống cũng như trong sản xuất. Các ứng dụng phổ biến của Zinc sulfide có thể kể đến như:
Zinc sulfide là một nguyên liệu quan trọng của phân bón và được sử dụng rộng rãi nhất để bổ sung kẽm cho cây trồng. Zn ảnh hưởng rất lớn đến sự hình thành nhiều loại hợp chất quan trọng trong cây như đường bột, protit, vitamin C, auxin, các phenol, tamin, các protein và enzym. Thiếu Zn dẫn tới hiện tượng lá non bị đốm vàng và vân lá có màu xanh tối.
Khi Zn được bổ sung sẽ giúp cây trồng tăng cường khả năng sử dụng và hấp thu phân đạm, phân lân trong cây, tăng khả năng chống chịu bệnh.
- Có tác dụng trong công nghiệp dệt may và nhuộm vải, in ấn.
- Được dùng như một chất kết tủa trong việc sản xuất tơ nhân tạo.
- Sử dụng trong quá trình tạo ra thuốc nhuộm màu cho vải, giúp thuốc nhuộm bám màu lâu hơn trên các sợi vải.
- Chúng còn là nguyên liệu để sản xuất mực in.
- Là một trong những loại thuốc thử hữu hiệu trong phòng thí nghiệm.
- Được dùng như chất tẩy rửa và chất khử để tẩy rỉ kim loại trước khi hàn, rửa chai lọ tổng hợp.
- Được dùng trong công nghiệp sản xuất muối vô cơ.
- Được thêm vào thức ăn cho gia súc gia cầm để bổ sung kẽm giúp động vật sinh trưởng khỏe mạnh hơn.
- Ngoài ra, trong làm gốm cũng không thể thiếu vắng được công dụng của kẽm sunfua.
Ứng dụng quan trọng của Zinc sulfide trong ngành nông nghiệp Việt Nam
Câu hỏi vận dụng liên quan
Câu 1. Khẳng định nào sau đây là đúng khi nói về tính chất hóa học của hiđro sunfua.
- Tính axit mạnh và tính khử yếu.
- Tính bazơ yếu và tính oxi hóa mạnh.
- Tính bazơ yếu và tính oxi hóa yếu.
- Tính axit yếu và tính khử mạnh
Xem đáp án
Câu 2. Cho khí H2S lội qua dung dịch CuSO4 thấy có kết tủa màu xám đen xuất hiện, chứng tỏ:
- Có phản ứng oxi hoá – khử xảy ra.
- Có kết tủa CuS tạo thành, không tan trong axit mạnh.
- Axit sunfuhiđric mạnh hơn axit sunfuric.
- Axit sunfuric mạnh hơn axit sunfuhiđric.
Xem đáp án
Câu 3. Cho các phản ứng: (1) Na2S + HCl ; (2) F2 + H2O; (3) MnO2 + HCl đặc; (4) Cl2 + dung dịch H2S.
Các phản ứng tạo ra đơn chất là
- (1), (2), (4).
- (2), (3), (4).
- (1), (2), (3).
- (1), (3), (4).
Xem đáp án
Câu 4. Trường hợp nào sau đây không xảy ra phản ứng hóa học?
- 3O2 + 2H2S → 2SO2 + 2H2O (to)
- FeCl2 + H2S → 2HCl + FeS
- O3+ 2KI + H2O → 2KOH + O2 + I2
- Cl2 + 2NaOH → NaCl + NaClO + H2O
Từ phản ứng ZnS ra H2S, chúng ta nhận thấy sự chuyển đổi từ chất rắn ZnS sang khí H2S. Quá trình này không chỉ là một biểu hiện của sự tương tác hóa học giữa các chất, mà còn là hệ quả của sự biến đổi và thích ứng trong tự nhiên. Nhìn thấy H2S thoát ra trong phản ứng, chúng ta nhớ về sự đa dạng và tính phong phú của các hiện tượng hóa học xung quanh chúng ta. Điều này khơi gợi cho chúng ta cảm hứng để tìm hiểu sâu hơn về cấu trúc và tính chất của các hợp chất, giúp mở rộng kiến thức và hiểu biết về thế giới hóa học đầy thú vị.
Xem thêm: