[Lưu ngay] Các công thức hóa học lớp 8 cần nhớ -Toppy
Hóa học thường là nỗi ám ảnh của không ít học sinh khi lên cấp 3. Đơn giản bởi bạn đã không biết cách học và ghi nhớ những kiến thức cơ bản ngay từ ban đầu đặc biệt là về công thức hóa học. Sau đây sẽ là tổng hợp các công thức hóa học lớp 8 cần nhớ để giúp bạn có cái nhìn toàn diện nhất về nền tảng hóa học để áp dụng vào học ở những năm tiếp theo.
Các công thức hóa học lớp 8 cần nhớ
Công thức hóa học lớp 8 mà bạn cần ghi nhớ bao gồm công thức tính số Mol và công thức tính nồng độ dung dịch. Sau đây sẽ là các công thức hóa học lớp 8 cần nhớ cụ thể.
Công thức tính số Mol
Tính số Mo1 theo khối lượng với công thức:
n = m/M
Trong đó:
- m: khối lượng
- M: khối lượng phân tử, khối lượng mol
Ví dụ 1
Cho 2,4 gam Mg vào dung dịch HCl dư. Tính thể tích khí hidro thu được ở điều kiện
chuẩn. (Cho Mg=24)
Tính số Mol theo thể tích (đối với chất khí ở điều kiện chuẩn):
n =V/22,4
Trong đó:
- V: thể tích khí
Ví dụ 2
Cho 6,75 gam kim loại nhôm vào dung dịch H2SO4 loãng . Phản ứng xong thu được
3,36 lít khí (đktc).
- Viết phương trình phản ứng.
- Tính khối lượng muối thu được sau phản ứng.
(Cho: Zn = 65; H = 1; S = 32; O = 16)
Công thức tính nồng độ dung dịch
Nồng độ mol /lít (CM)
Một trong số các công thức cần nhớ tiếp theo là:
CM =n/V (M)
Trong đó:
- N: số mol chất tan trong dung dịch (mol)
- V: thể tích dung dịch
>> Đăng ký học thử miễn phí môn Hóa học từ lớp 8 đến lớp 12
Ví dụ 3
Để trung hòa hết 200 gam dung dịch NaOH 10% cần dùng bao nhiêu gam dung dịch HCl 3,65%.
(cho Na = 23; Cl = 35,5; O = 16; H = 1)
Ví dụ 4
Cho 200ml dung dịch NaOH 8% có D = 1,15g/ml tác dụng với 380 gam dung dịch MgCl2 5%.
- Viết PTHH. Chất nào còn dư? Tính khối lượng chất dư.
- Tính khối lượng kết tủa tạo thành. Sau khi loại bỏ kết tủa, tính C% các chất còn lại sau phản ứng.
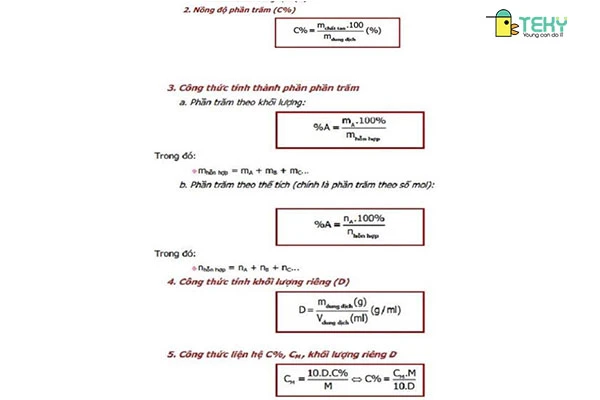
Như vậy có thể tổng hợp các công thức hóa học lớp 8 cần nhớ như sau:
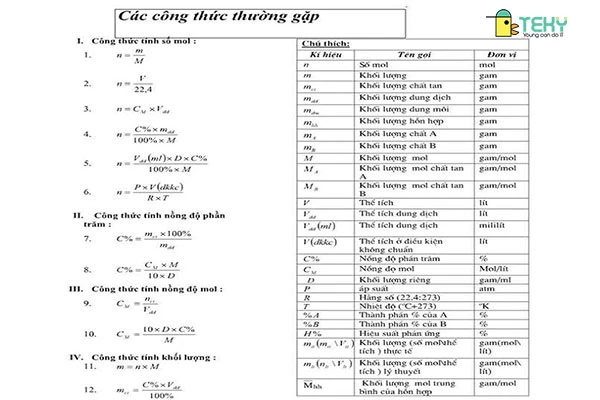
Các công thức hóa học 8 cần nhớ theo từng chuyên đề trong SGK
Trong SGK Hóa học 8 có 4 chuyên đề với 4 nội dung khác nhau và các công thức hóa học cũng như kiến thức trọng tâm bạn cần nhớ là:
Phần 1: Chất – Nguyên tử
Kiến thức trọng tâm về Chất
Chất tồn tại ở khắp nơi. Ở đâu có vật thể thì ở đó có chất.
Vật thể sẽ do 1 hoặc nhiều chất tạo nên.
Mỗi chất sẽ có tính chất hóa học và vật lý khác nhau.
Hỗn hợp là sản phẩm do hai hay nhiều chất trộn vào với nhau.
Tách chất ra khỏi hỗn hợp bằng cách dựa vào tính chất vật lý và hóa học của từng chất.
Kiến thức trọng tâm về Nguyên tử
Nguyên tử là hạt vô cùng nhỏ và trung hòa về điện.
Cấu tạo của nguyên tử sẽ gồm: vỏ nguyên tử và hạt nhân nguyên tử
Hạt nhân nguyên tử gồm: hạt proton mang điện tích dương, hạt electron mang điện tích âm và hạt nơtron không mang điện.

Đặc điểm và công thức của hạt nhân nguyên tử
- Số proton bằng số electron vì thế nguyên tử trung hòa về điện nên. Công thức p = e.
- Electron luôn luôn chuyển động xung quanh hạt nhân và chúng sắp xếp thành từng lớp.
- Proton và notron sẽ có cùng khối lượng với nhau. Công thức: m (p) = m (n)
- Khối lượng của electron rất bé không đáng kể, Nên khối lượng nguyên tử cũng là khối lượng hạt nhân với công thức: m (nguyên tử) = m (hạt nhân)
Kiến thức trọng tâm về Nguyên tố hóa học
Nguyên tố hóa học: Là tập hợp những nguyên tử cùng loại. Chúng sẽ có cùng số proton trong hạt nhân. Ký hiệu của các nguyên tố hóa học là khác nhau. Ví dụ: Na, K, S, Cl, Fe
Nguyên tử khối là khối lượng của một nguyên tử tính bằng đơn vị cacbon. Mỗi nguyên tử có một khối lượng riêng biệt,
Đơn vị cacbon (đvC): 1 đvC = 1/12 m (Cacbon)
Trong đó khối lượng nguyên tử C – m (Cacbon) = 1, 9926. 10 -23
Phần 2: Phân tử
Phân tử chính là đại diện cho một chất. Chúng gồm một số nguyên tử liên kết với nhau và thường thể hiện tính chất hóa học của chất đó.
Các công thức hóa học lớp 8 cần nhớ của phân tử là:
- Đơn chất gồm một nguyên tố hóa học. Ví dụ: H2, O2…
- Hợp chất là chất được tạo nên từ hai nguyên tố hóa học trở lên. Ví dụ: NaCl, MnO, H2O…
Như vậy chúng ta có công thức tính khối lượng phân tử như sau:
Phân tử khối = khối lượng phân tử (đvC) = tổng số nguyên tử nguyên tố . nguyên tử khối
>> Bật mí cách đánh bay nỗi sợ môn Hóa học – Toppy
Phần 3: Công thức hóa học
Công thức hóa học cũng là một nhóm kiến thức vô cùng quan trọng của lớp 8. Các công thức cần nhớ và kiến thức của phần này là:
Công thức hóa học của một đơn chất sẽ được kí hiệu dưới 2 dạng là A và Ax. Trong đó
- A là đơn chất kim loại và một vài phi kim. Ví dụ như: Na, Fe, Cu, P, C, S
- Ax là đơn chất phi kim sẽ bao gồm 2 nguyên tử liên kết với nhau như: O2, H2, N2
Công thức hóa học của các hợp chất là: AxByCz
Trong đó:
- A, B, C: các kí hiệu hóa học
- x, y, z là các chỉ số chân cho bạn biết về số nguyên tử của nguyên tố đó có trong một phân tử là bao nhiêu
Phần 4: Hóa trị
Hóa trị của một hoặc một nhóm nguyên tố là con số được viết bên cạnh tên của nguyên tố đó. Chúng biểu thị cho khả năng liên kết của các nguyên tử hoặc nhóm nguyên tử đó.
Quy tắc hóa trị: AxBy -> a.x = b.y
Trong đó
- a, b là hóa trị của nguyên tố.
- x, y là chỉ số hay số nguyên tử của nguyên tố
Trên đây là các công thức hóa học lớp 8 cần nhớ hy vọng đã có thể giúp bạn khái quát lại toàn bộ kiến thức môn hóa lớp 8 để bạn học tập dễ dàng hơn.
Xem thêm:
- Tính chất vật lý của Kim loại – Học tốt Hóa 9
- Dãy hoạt động hóa học của kim loại đầy đủ lớp 9
- Tính chất hóa học của phi kim – Những lưu ý khi học
Giải pháp toàn diện giúp con đạt điểm 9-10 dễ dàng cùng Toppy
Với mục tiêu lấy học sinh làm trung tâm, Toppy chú trọng việc xây dựng cho học sinh một lộ trình học tập cá nhân, giúp học sinh nắm vững căn bản và tiếp cận kiến thức nâng cao nhờ hệ thống nhắc học, thư viện bài tập và đề thi chuẩn khung năng lực từ 9 lên 10.
Kho học liệu khổng lồ
Kho video bài giảng, nội dung minh hoạ sinh động, dễ hiểu, gắn kết học sinh vào hoạt động tự học. Thư viên bài tập, đề thi phong phú, bài tập tự luyện phân cấp nhiều trình độ.Tự luyện – tự chữa bài giúp tăng hiệu quả và rút ngắn thời gian học. Kết hợp phòng thi ảo (Mock Test) có giám thị thật để chuẩn bị sẵn sàng và tháo gỡ nỗi lo về bài thi IELTS.

Nền tảng học tập thông minh, không giới hạn, cam kết hiệu quả
Chỉ cần điện thoại hoặc máy tính/laptop là bạn có thể học bất cứ lúc nào, bất cứ nơi đâu. 100% học viên trải nghiệm tự học cùng TOPPY đều đạt kết quả như mong muốn. Các kỹ năng cần tập trung đều được cải thiện đạt hiệu quả cao. Học lại miễn phí tới khi đạt!
Tự động thiết lập lộ trình học tập tối ưu nhất
Lộ trình học tập cá nhân hóa cho mỗi học viên dựa trên bài kiểm tra đầu vào, hành vi học tập, kết quả luyện tập (tốc độ, điểm số) trên từng đơn vị kiến thức; từ đó tập trung vào các kỹ năng còn yếu và những phần kiến thức học viên chưa nắm vững.
Trợ lý ảo và Cố vấn học tập Online đồng hành hỗ trợ xuyên suốt quá trình học tập
Kết hợp với ứng dụng AI nhắc học, đánh giá học tập thông minh, chi tiết và đội ngũ hỗ trợ thắc mắc 24/7, giúp kèm cặp và động viên học sinh trong suốt quá trình học, tạo sự yên tâm giao phó cho phụ huynh.