NaCl ra HCl | Phương trình NaCl rắn + H2SO4 đặc → NaHSO4 + HCl

Phản ứng biến đổi NaCl ra HCl đã thu hút sự chú ý của các nhà khoa học trong những năm gần đây. Quá trình này đang tạo ra những tiềm năng vượt bậc trong ngành công nghiệp và nông nghiệp. Từ việc tối ưu hóa quá trình sản xuất, giảm chi phí đến ứng dụng trong xử lý nước, sự chuyển đổi này hứa hẹn mang lại những đột phá đáng kể. Hãy cùng khám phá thêm về ứng dụng và lợi ích của việc NaCl ra HCl.
Lý thuyết về nội dung NaCl ra HCl
Phương trình điều chế NaCl ra HCl
NaCl + H2SO4 –> NaHSO4 + HCl
Điều kiện phản ứng NaCl tác dụng H2SO4 đặc
Nhiệt độ < 250oC
Cách tiến hành phản ứng NaCl tác dụng H2SO4 đặc
Cho tinh thể NaCl tác dụng với H2SO4 đặc và đun nóng
Nội dung mở rộng NaCl ra HCl
Định nghĩa NaCl là muối gì?
Vậy định nghĩa cụ thể NaCl là muối gì? “Natri clorua là một hợp chất vô cơ có công thức hóa học là NaCl. Đây là muối chủ yếu tạo ra độ mặn trong các đại dương và chất lỏng ngoại bào của nhiều cơ thể đa bào. Đây cũng là thành phần chính trong muối ăn được sử dụng phổ biến làm gia vị hay chất bảo quản thực phẩm”.
Nguồn gốc của NaCl:
Để hiểu rõ bản chất của NaCl là muối gì? Các bạn cũng cần tìm hiểu rõ nguồn gốc của chúng.
Thực tế, NaCl có nguồn gốc chủ yếu từ đất liền là nước ngọt từ các cơn mưa không ở dạng tinh khiết 100% hòa tan CO2 trong khí quyển rơi xuống đất. Khi nước mưa chảy trên mặt đất để tiếp cận đường thoát nước trong khu vực, tính axit của nước mưa phá vỡ đá, thu giữ ion trong đá sau đó mang chúng ra biển. Trong đó, 90% các ion này là natri hoặc clo, chúng kết hợp với nhau tạo thành muối. Một phần nhỏ khác muối có nguồn gốc từ miệng núi lửa hoặc đá ở trên đáy biển.
Cấu trúc tinh thể của muối NaCl:
Natri chloride tạo thành các tinh thể có cấu trúc cân đối lập phương. Trong các tinh thể này, các anion clorua lớn được sắp xếp trong khối khép kín lập phương, trong khi các cation natri nhỏ hơn lấp vào các lỗ hổng bát diện giữa chúng. Mỗi ion được bao quanh bởi 6 ion khác loại. Cấu trúc cơ bản như thế này cũng được tìm thấy trong nhiều khoáng chất khác và được biết đến như là cấu trúc halide.

Cách đọc tên muối NaCl
Muối có rất nhiều tên gọi khác nhau như natri clorua, muối, muối ăn, muối mỏ, hay halide. Liên minh Quốc tế về Hóa học cơ bản và Hóa học ứng dụng (IUPAC – International Union of Pure and Applied Chemistry), tên gọi chính thức của NaCl là Natri Clorua.
Tính chất vật lý của Nacl là gì?
Tìm hiểu NaCl là muối gì không thể không nhắc đến tính chất vật lý của nó. NaCl là muối phổ biến với những tính chất vật lý đặc trưng sau:
- Muối Nacl là chất rắn kết tinh màu trắng hoặc không màu.
- Muối NaCl không có mùi.
- Muối NaCl là chất hút ẩm trong tự nhiên. Nó hấp thụ độ ẩm từ khí quyển ẩm trên 75% độ ẩm tương đối và dưới mức này sẽ khô.
- Nhiệt độ nóng chảy của muối NaCl rất cao, ở 801 độ C và bắt đầu bốc hơi ở nhiệt độ ngay trên điểm sôi 1413 độ C.
- Độ hòa tan trong nước của muối là 35.9g.ml (25 độ C). Độ tan của muối NaCl ở trong nước giảm xuống khi có sự hiện diện của NaOH, CaCl2, HCl, MgCl2…
- Tương tự như các muối ion khác, muối NaCl có khả năng dẫn điện và dẫn nhiệt ở trạng thái lỏng và dung dịch nhưng không thể khi tồn tại ở trạng thái rắn.
- Muối NaCl cũng rất ít tan trong rượu, không hòa tan trong axit clohydric (HCl) đậm đặc. Đây vừa là tính chất vật lý, vừa là tính chất hóa học đáng chú ý của muối NaCl.

Tính chất hóa học của muối NaCl
Tìm hiểu định nghĩa NaCl là muối gì, ngoài tính chất vật lý, chúng ta cần hiểu về tính chất hóa học của nó.
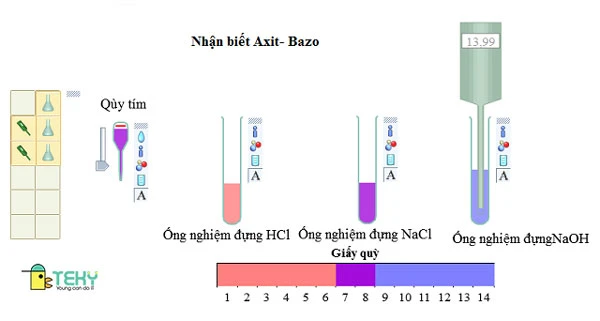
- Loại muối: NaCl là muối trung hòa – muối mà anion gốc Axit không có khả năng phân li ra ion H+. NaCl có pH = 7 và nó không đổi màu quỳ tím.
- Liên kết hóa học: NaCl là một liên kết hóa học có bản chất là lực hút tĩnh điện giữa hai ion mang điện tích trái dấu, ở đây là Na+ và Cl–. Liên kết ion được hình thành do lực hút tĩnh điện giữa kim loại điển hình và phi kim điển hình.
- Sự điện li: NaCl là chất điện li mạnh, phân li hoàn toàn trong nước, tạo ra các ion âm và dương, là ion Na+ và Cl–.
- Sự kết tủa: Khi cho HCl đặc vào dung dịch bão hòa Natri Clorua sẽ tạo thành kết tủa trắng. Khi thêm nước vào hỗn hợp này, kết tủa sẽ hòa tan lại.
- Các phản ứng tiêu biểu: NaCl không phản ứng với kim loại, axit, bazơ ở điều kiện thường. Tuy nhiên, NaCl vẫn phản ứng với một muối.

Sản xuất và điều chế muối NaCl như thế nào?
Sản xuất và điều chế muối NaCl có ý nghĩa quan trọng trong sản xuất và đời sống.
Trạng thái tự nhiên:
- Cho nước biển bay hơi nước, ta được chất rắn là hỗn hợp của nhiều muối, thành phần chính là natri clorua (trong 1m3 nước biển có hòa tan khoảng 27 kg muối natri clorua, 5kg muối magie clorua, 1kg muối canxi sunfat và một khối lượng nhỏ những muối khác).
- Ngoài ra, trong lòng đất cũng chứa một lượng lớn muối natri clorua kết tinh, được gọi là muối mỏ. Mỏ muối có nguồn gốc từ những hồ nước mặt có trước đây hàng triệu năm. Nước hồ bị bay hơi, còn lại là muối natri clorua kết tinh thành những vỉa dầy trong lòng đất (Theo SGK Hóa học 9, NXB giáo dục Việt Nam).
Cách khai thác muối:
- Ở những nước có biển hoặc hồ nước mặn, người ta thường khai thác NaCl từ nước mặn ở trên. Cho nước mặn bay hơi từ từ, thu được muối kết tinh.
- Ở những nơi có mỏ muối, người ta khai thác muối bằng cách đào hầm hoặc giếng sâu qua các lớp đất đá đến mỏ muối. Muối mỏ sau khi khai thác được nghiền nhỏ và tinh chế để có muối sạch.

Bài tập vận dụng liên quan NaCl ra HCl
Câu 1. Khí hidro clorua có thể được điều chế bằng cách cho muối ăn (NaCl rắn) tác dụng với chất nào sau đây?
A. H2SO4 loãng.
B. H2SO4 đặc.
C. NaOH đặc
D. H2O.
Câu 2. Dãy chất nào dưới đây phản ứng được với dung dịch H2SO4 loãng
A. Cu, NaOH, KCl
B. Fe, KOH, BaCl2
C. Ag, NaOH, NaCl
D. Mg, KOH, SO2
Câu 3. Hòa tan hoàn toàn 2,55 gam hỗn hợp X gồm Fe, Mg và Zn bằng 1 lượng vừa đủ dung dịch H2SO4 loãng, thu được 2,24 lít khí hidro (đktc) và dung dịch chứa m gam muối. Giá trị của m là
A. 9,52
B. 10,27
C. 12,35
D. 12,15
Đáp án D
nH2 = 2,24/22,4 = 0,1 (mol) ⇒ nH2SO4 = nH2 = 0,1 mol
Bảo toàn khối lượng: 2,55 + 0,1.98 = m + 0,1.2
m = 12,15 gam
Câu 4. Axit H2SO4 đặc có thể làm khô khí nào sau đây là tốt nhất?
A. H2S
B. SO3
C. CO2
D. BaO
……………………………..
Kết thúc của quá trình NaCl ra HCl đánh dấu một bước tiến quan trọng trong lĩnh vực hóa học hiện đại. Sự biến đổi này mang đến không chỉ hiệu quả kinh tế mà còn thúc đẩy sự phát triển bền vững. Nhờ nó, các ngành công nghiệp và nông nghiệp đã trải qua sự đổi mới đáng kể, tạo ra những sản phẩm và dịch vụ tiên tiến hơn. Nhìn vào tương lai, việc NaCl ra HCl còn hứa hẹn mang lại nhiều khám phá mới và ứng dụng tiềm năng chưa từng thấy.
Xem thêm: