NaHCO3 + HCl | Phương trình NaHCO3 + HCl → NaCl + CO2 + H2O

Phản ứng giữa NAHCO3 + HCl là một trong những phản ứng hóa học quan trọng và thú vị. Khi hai chất này tương tác với nhau, tạo ra khí CO2, nước, muối. Hiện tượng này thường được thấy trong cuộc sống hàng ngày, như trong quá trình nấu ăn và làm bánh. Đồng thời, phản ứng NAHCO3 + HCl cũng có ứng dụng trong y học và các ngành công nghiệp khác. Hãy cùng tìm hiểu thêm về sự quan trọng và ứng dụng của phản ứng này.
Lý thuyết về NAHCO3 + HCl
Phương trình HCl tác dụng với NaHCO3
NaHCO3 + HCl → NaCl + CO2 + H2O
Điều kiện phản ứng HCl tác dụng với NaHCO3
Không có
Cách thực hiện phản ứng HCl tác dụng với NaHCO3
Cho HCl vào ống nghiệm đựng dung dịch NaHCO3
Hiện tượng nhận biết
Cho HCl vào ống nghiệm đựng dung dịch NaHCO3 sau phản ứng Có bọt khí thoát ra là CO2
Muối cacbonat tác dụng với dung dịch axit mạnh hơn axit cacbonic tạo thành muối mới và giải phóng CO2
Tính chất hóa học của NaHCO3
- Nhiệt phân tạo thành muối và giải phóng CO2
Tiến hành nhiệt phân hóa chất soda baking sẽ tạo ra muối mới và giải phóng khí CO2. Phương trình phản ứng như sau:
2NaHCO3 → Na2CO3 + CO2↑ + H2O
- Thủy phân tạo thành môi trường Bazơ yếu
Phản ứng với nước, NaHCO3 sẽ bị thủy phân tạo ra môi trường bazơ yếu.
NaHCO3 + H2O → NaOH + H2CO3
- Tác dụng với axit mạnh tạo thành muối và nước
Khi được sử dụng, hoặc tiếp xúc với các axit mạnh, NaHCO3 sẽ tạo thành dung dịch muối và nước, đồng thời giải phóng khí CO2.
Tác dụng với Axit Sunfuric:
2NaHCO3 + H2SO4 → Na2SO4 + 2H2O + 2CO2
Tác dụng với axit Clohiric:
NaHCO3 + HCl → NaCl + H2O + CO2
- Tác dụng với bazơ tạo thành muối mới và bazơ mới
Khi được tác dụng với bazơ, NaHCO3 sẽ tạo ra muối mới và bazơ mới. Phương trình phản ứng như sau:
Tác dụng với Ca(OH)2
NaHCO3 + Ca(OH)2 → CaCO3 + NaOH + H2O.
Một trường hợp khác có thể tạo thành 2 muối mới với phương trình phản ứng:
2NaHCO3 + Ca(OH)2 → CaCO3 + Na2CO3 + 2H2O.
Tác dụng với NaOH:
NaHCO3 + NaOH → H2O + Na2CO3
Tác dụng với Ba(OH)2
2NaHCO3 + Ba(OH)2 → Na2CO3 + Ba2CO3 + 2H2O
Nội dung mở rộng NAHCO3 + HCL
Thí nghiệm nhiệt phân NaHCO3
NaHCO3 – Natri bicacbonat (Hay còn gọi là baking soda) là chất rắn màu trắng, thường có dạng tinh thể. Hợp chất này khá giống bột, vị hơi mặn và có tính kiềm tương tự như một số loại soda sử dụng trong tẩy rửa (đặc biệt là Na2CO3). Vì thế có thể sử dụng baking soda này như một chất tẩy rửa. Về tính chất, khác với một số loại muối hidrocacbonat hoặc muối của các kim loại kiềm, baking soda thường ít tan trong nước và trong một số trường hợp có thể coi là không tan.
Phản ứng nhiệt phân NaHCO3 là phản ứng đặc biệt thể hiện tính chất hóa học đặc trưng của hợp chất. Đồng thời, đây là giải pháp để chuyển hóa NaHCO3 ra Na2CO3 hiệu quả và nhanh chóng. Quá trình này thường tạo ra lượng nhiệt rất lớn. Mời các bạn tham khảo chi tiết thí nghiệm được thực hiện bởi đội ngũ KTV của Bilico.
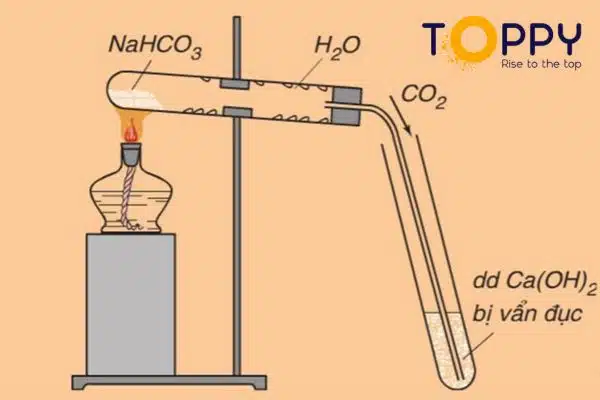
Thí nghiệm nhiệt phân NaHCO3
Thí nghiệm
Chuẩn bị: Để thực hiện thí nghiệm nhiệt phân NaHCO3 cần chuẩn bị các dụng cụ cần thiết bao gồm
- Ống nghiệm
- Cốc
- Đèn cồn
- Giá đỡ
- Ống dẫn khí
- Các hóa chất cần thiết bao gồm: Muối NaHCO3 và dung dịch Ca(OH)2.
Hình ảnh các dụng cụ cần chuẩn bị
Hướng dẫn cách thực hiện
- Bước 1: Thực hiện lấy 1 thìa muối NaHCO3 và cho vào trong ống nghiệm đã chuẩn bị sẵn trước đó.
- Bước 2: Đậy nắp ống nghiệm. Lưu ý nên sử dụng nắp ống nghiệp bằng chất liệu cao su.
- Bước 3: Tiến hành châm lửa đèn cồn.
- Bước 4: Cầm đèn cồn hơ nóng toàn bộ ống nghiệm sau đó đặt đèn cồn ở vị trí đáy của ống nghiệm vừa bỏ muối NaHCO3.
- Bước 5. Tiến hành quan sát thí nghiệm.
Chi tiết các bước thực hiện thí nghiệm nhiệt phân natri hidrocacbonat
Kết quả thí nghiệm
Sau khi thực hiện thí nghiệm nhiệt phân NaHCO3 bằng ống nghiệp ta sẽ thu được kết quả bằng các hiện tượng như sau:
- Thành của ống nghiệm có xuất hiện nhiều giọt nước đọng lại.
- Ống nghiệm có hiện tượng vẩn đục.
Kết hợp với quá trình nhiệt phân, trong ống nghiệp sẽ tiếp tục xảy ra phản ứng giữa khí CO2 và dung dịch Ca(OH)2. Hiện tượng vẩn đục này là sự xuất hiện của hỗn hợp các chất: Muối Na2CO3, nước và khí CO2. Như vậy, có thể coi, phản ứng nhiệt phân muối NaHCO3 là một cách để điều chế muối natri cacbonat (Na2CO3) vô cùng hiệu quả. Vậy cụ thể phương trình phản ứng ra sao?
Phương trình phản ứng nhiệt phân NaHCO3 ra Na2CO3
- Phương trình nhiệt phân
Khi có tác dụng của nhiệt độ, NaHCO3 sẽ có sự chuyển hóa thành Na2CO3 với phương trình phản ứng như sau:
2NaHCO3 → Na2CO3 +CO2↑ + H2O
- Bên cạnh đó trong thí nghiệm nói trên sẽ xảy ra một phản ứng khác như sau:
CO2 + Ca(OH)2 → CaCO3 + H2O
Ứng dụng nhiệt phân NaHCO3 ra Na2CO3 như thế nào?
- Nhiệt phân NaHCO3 ra Na2CO3 sẽ giải phóng ra khí CO2 (tên thường gọi là khí cacbonic hay cacbon đioxit), vì thế chúng được sử dụng nhiều trong việc nấu ăn và tạo xốp cho các loại bánh sau đây:
- Bánh muffin
- Bánh cookies
- Bánh biscuits
- Bánh quẩy
- Sử dụng trong một số loại nước giải khát, nước chanh để làm giảm nồng độ axit. Ít ai biết baking soda nếu sử dụng hàm lượng vừa đủ với nước ngâm đậu sẽ giúp giảm thời gian chế biến và tăng độ mềm cho sản phẩm.
- Baking soda cũng khá hiệu quả khi được sử dụng với các món thịt hầm. Nguyên nhân là khi chuyển hóa NaHCO3 ra Na2CO3 và giải phóng khí Cacbonic. Khí này sẽ kết hợp với nước tạo ra tính axit ngấm và làm mềm loại thực phẩm đang ninh, nấu.
Ứng dụng nhiệt phân NaHCO3 ra Na2CO3
Bài tập vận dụng liên quan
Câu 1. Cho các phát biểu sau :
(1) Có thể tìm được kim loại kiềm ở dạng nguyên chất ở những mỏ nằm sâu trong lòng đất.
(2) Trong cùng một chu kì của bảng tuần hoàn, kim loại kiềm có tính khử mạnh nhất.
(3) Trong bảng tuần hoàn, đi từ trên xuống dưới trong một nhóm, nhiệt độ nóng chảy của các kim loại tăng dần.
(4) Trong bảng tuần hoàn, đi từ trên xuống dưới trong một nhóm, nhiệt độ sôi của các kim loại giảm dần.
(5) Kim loại kiềm đều là những kim loại nhẹ hơn nước.
Trong các phát biểu trên, số phát biểu đúng là:
- 2
- 3.
- 4.
- 5.
Đáp án A
(2) Trong cùng một chu kì của bảng tuần hoàn, kim loại kiềm có tính khử mạnh nhất.
(4) Trong bảng tuần hoàn, đi từ trên xuống dưới trong một nhóm, nhiệt độ sôi của các kim loại giảm dần.
Câu 2. Khi cho kim loại Na vào dung dịch CuSO4 thì sẽ xảy ra hiện tượng nào sau đây?
- Ban đầu có xuất hiện kết tủa xanh, sau đó kết tủa tan ra, dung dịch trong suốt.
- Ban đầu có sủi bọt khí, sau đó xuất hiện kết tủa xanh.
- Ban đầu có sủi bọt khí, sau đó có tạo kết tủa xanh, rồi kết tủa tan ra, dung dịch trong suốt.
- Chỉ có sủi bọt khí.
Đáp án B: Ban đầu, Na sẽ tác dụng với nước trước tạo NaOH và sủi bọt khí, sau đó có kết tủa xanh và không tan
Câu 3. Cho 3,36 gam hỗn hợp gồm K và một kim loại kiềm A vào nước thấy thoát ra 1,792 lít H2. Thành phần phần trăm về khối lượng của A là
- 18,75 %.
- 10,09%.
- 13,13%.
- 55,33%.
Đáp án A
Gọi công thức tổng quát chung của 2 kim loại kiềm là M
Phương trình phản ứng xảy ra
M + H2O → MOH + 1/2 H2
nM = 2nH2 = 1,792/22,4 = 0,16 mol => M = 3,36/0,16 = 21
Ta có Li (7) < M = 21 < K (39)
Gọi x, y lần lượt là số mol của K và Li
Ta có:
39 x + 7y = 3,36 => x = 0,07 mol, y = 0,09 mol
x + y = 0,16
%mLi = 0,09.7/3,36.100% = 18,75%
Câu 4. Phát biểu nào sau đây là sai khi nói về 2 muối NaHCO3 và Na2CO3?
- Cả 2 muối đều dễ bị nhiệt phân.
- Cả 2 muối đều tác dụng với axit mạnh giải phóng khí CO2.
- Cả 2 muối đều bị thủy phân tạo mỗi trường kiềm yếu.
- Cả 2 muối đều có thể tác dụng với dung dịch Ca(OH)2 tạo kết tủa.
Đáp án A
Câu 5. Nhỏ từ từ từng giọt đến hết 30 ml dung dịch HCl 1M vào 100 ml dung dịch chứa Na2CO3 0,2M và NaHCO3 0,2M, sau phản ứng thu được số mol CO2 là
- 0,020.
- 0,030.
- 0,015.
- 0,010.
Đáp án D
Nhỏ từ từ HCl vào dung dịch thứ tự phản ứng:
H+ + CO32- → HCO3– (1)
H+ + HCO3– → CO2 + H2O (2)
nH+ = 0,03 mol
nCO32- = 0,02 mol < nH+
nH+ (2) = nCO2 = 0,03 – 0,02 = 0,01 mol
Câu 6. Cho các chất sau: NaCl, Ca(OH)2, Na2CO3, HCl, NaHSO4. Số chất có thể làm mềm nước cứng tạm thời là
- 4
- 3
- 1
- 2
Đáp án D
Câu 7. Nhỏ từ từ từng giọt đến hết 60 ml dung dịch HCl 1M vào 200 ml dung dịch chứa Na2CO3 0,2M và NaHCO3 0,2M, sau phản ứng thu được số mol CO2 là
- 0,020.
- 0,030.
- 0,015.
- 0,010.
Đáp án A
Nhỏ từ từ HCl vào dung dịch thứ tự phản ứng:
H+ + CO32- → HCO3– (1)
H+ + HCO3– → CO2 + H2O (2)
nH+ = 0,06 mol
nCO32- = 0,04 mol < nH+
nH+ (2) = nCO2 = 0,06 – 0,04 = 0,02 mol
Câu 8. Hỗn hợp X chứa K2O, NH4Cl, KHCO3 và BaCl2 với số mol các chất bằng nhau. Cho hỗn hợp X vào nước dư và đun nóng. Các chất tan trong dung dịch thu được là:
- KCl, KOH, BaCl2.
- KCl, KOH.
- KCl, KHCO3, NH4Cl, BaCl2.
- KCl.
Đáp án D
Phản ứng xảy ra khi hỗn hợp tác dụng với nước:
K2O + H2O → 2KOH
Các phản ứng xảy ra tiếp theo:
NH4Cl + KOH → NH3 + H2O + KCl
KHCO3 + KOH → K2CO3 + H2O
K2CO3 + BaCl2 → BaCO3 + KCl
Vậy sau phản ứng dung dịch còn lại KCl
Câu 12. Dãy oxit tác dụng với dung dịch H2SO4 loãng là:
- MgO, Fe2O3, SO2, CuO.
- Fe2O3, MgO, P2O5, K2O .
- MgO, Fe2O3, CuO, K2O.
- MgO, Fe2O3, SO2, P2O5.
Đáp án C
MgO + H2SO4 → MgSO4 + H2O
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
CuO + H2SO4 → CuSO4 + H2O
K2O + H2SO4 → K2SO4 + H2O
Câu 13.Dãy các chất tác dụng với lưu huỳnh đioxit là:
- Na2O, CO2, NaOH, Ca(OH)2
- CaO, K2O, KOH, Ca(OH)2
- HCl, Na2O, Fe2O3, Fe(OH)3
- Na2O, CuO, SO3, CO2
Đáp án B
Câu 14. Khí sunfurơ được tạo ra từ cặp chất nào sau đây?
- Muối natri sunfit và axit cacbonic
- Muối natri sunfit và dung dịch axit clohiđric
- Muối natri sunfat và dung dịch axit clohiđric
- Muối natri sunfat và muối đồng(II) clorua
Đáp án B
Câu 15. Dung dịch Ca(OH)2 phản ứng với dãy chất nào sau đây?
- BaCl2, K2CO3, Al.
- CO2, K2CO3, Ca(HCO3)2.
- NaCl, K2CO3, Ca(HCO3)2.
- NaHCO3, NH4NO3, MgCO3.
Đáp án B
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
K2CO3 + Ca(OH)2 → CaCO3 ↓ + 2NaOH.
Ca(HCO3)2 + Ca(OH)2 → 2CaCO3 ↓ + 2H2O
Câu 16. Khi nung 60 gam hỗn hợp CaCO3 và MgCO3 thì khối lượng chất rắn thu được sau phản ứng chỉ bằng một nửa khối lượng ban đầu. Thành phần % theo khối lượng các chất ban đầu là
- 28,33% và 71,67%.
- 40,00% và 60,00%.
- 13,00% và 87,00%.
- 50,87% và 49,13%.
Đáp án A
Gọi số x, y lần lượt là số mol CaCO3 và MgCO3 trong hỗn hợp
Ta có: 100x + 84y = 60 (1)
Phương trình hóa học:
CaCO3 → CaO + CO2
x → x → x
MgCO3 → MgO + CO2
y → y → y
Áp dụng định luật bảo toàn khối lượng:
mhh trước = mcr sau + mkhí → mkhí = 60 – 30 = 30 gam.
→ nkhí = 30/44 → x + y = 30/44.
Giải hệ có x = 0,17 và y = 0,452
%mCaCO3 = (0,17.100)/60 .100 = 28,33%
%mMgCO3 = 100% – 28,33% = 71,67%
……………………………
Kết luận của phản ứng NAHCO3 + HCl là một phần quan trọng trong lĩnh vực hóa học và ứng dụng. Sự tương tác giữa hai chất này tạo ra khí CO2, nước và muối, có tên gọi là muối bicarbonate. Hy vọng phản ứng này sẽ giúp chúng ta khám phá thêm về các ứng dụng tiềm năng và phát triển sáng tạo trong tương lai.
Xem thêm: