So2 ra S | Cân bằng phản ứng SO2 + H2S → S + H2O

SO2 + H2S → S + H2O được Topy biên soạn hướng dẫn các bạn học sinh viết phương trình hóa học từ SO2 ra S. Đây là phương trình phản ứng thể hiện lưu huỳnh đioxit là chất oxi hóa khi cho SO2 tác dụng với H2S. Mời các học sinh tham khảo thông tin chi tiết bên dưới.
Phương trình hóa học So2 ra S
1. Phản ứng So2 ra S
SO2 + 2H2S → 3S↓ + 2H2O
SO2 là chất oxi hóa (bị khử) và H2S là chất khử (bị oxi hóa)
2. Điều kiện phản ứng SO2 ra S
Nhiệt độ thường
Bạn đang xem: SO2 + H2S → S + H2O
3. Hiện tượng phản ứng giữa So2 ra S
Xuất hiện kết tủa vàng Lưu huỳnh (S)
Nội dung mở rộng
1. Lưu huỳnh là gì?
Lưu huỳnh còn có tên khác là sulfur, lưu hoàng hay diêm sinh. Đây là một nguyên tố nằm trong bảng tuần hoàn hóa học có ký hiệu S và số nguyên tử 16. Lưu huỳnh là một phi kim không mùi, không vị, nhiều hóa trị. Dạng gốc của lưu huỳnh là chất rắn kết tinh màu vàng chanh, được xem là một nguyên tố thiết yếu cho sự sống và chúng được tìm thấy trong 2 axit amin.
Lưu huỳnh có ở đâu?
-
Trong tự nhiên, lưu huỳnh có thể được tìm thấy ở dạng đơn chất, trong các khoáng chất sulfua và sulfat.
-
Lưu huỳnh dạng đơn chất xuất hiện xung quanh các suối nước nóng, các khu vực núi lửa tại nhiều nơi trên thế giới, đặc biệt là khu vực dọc theo vành đai lửa Thái Bình Dương.
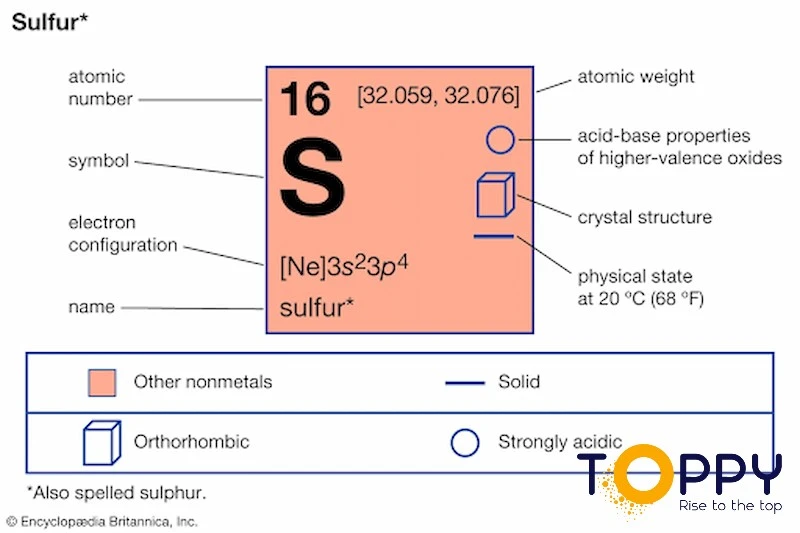
Số hiệu nguyên tử: 16
Vị trí: thuộc nhóm VIA, chu kì 3 trong bảng tuần hoàn các nguyên tố hóa học.
Cấu hình e: 1s22s22p63s23p4 với 6 e lớp ngoài cùng.
2. Những tính chất vật lý của lưu huỳnh
Lưu huỳnh mang những tính chất vật lý sau đây:

-
Trạng thái: Ở nhiệt độ phòng, lưu huỳnh là một chất rắn xốp có màu vàng nhạt. Lưu huỳnh trong trạng thái này thông thường tồn tại như các phân tử vòng dạng vòng hoa S8.
-
Tinh thể: Lưu huỳnh có tinh thể rất phức tạp, phụ thuộc vào các điều kiện khác nhau. Các dạng hình thù của chúng tạo thành các cấu trúc tinh thể khác nhau, có thể là các dạng hình thoi và xiên đơn S8 là các dạng tinh thể được nghiên cứu tỉ mỉ nhất.
-
Mùi: Lưu huỳnh không được ưa thích do mùi của nó khá giống với mùi trứng ung – đây là đặc trưng của hydro sulfide (H2S). Lưu huỳnh đơn chất không có mùi. Khi cháy, nó tạo ra ngọn lửa màu xanh lam và tỏa ra lưu huỳnh dioxide – một mùi ngột ngạt khác thường.
-
Khả năng hòa tan: Lưu huỳnh không hòa tan trong nước nhưng lại hòa tan được trong cacbon disulfide và các dung môi không phân cực khác.
-
Các mức oxi hóa: Lưu huỳnh có các mức oxi hóa là: -2, -1 (pirit sắt…), +2, +4, +6. Lưu huỳnh có khả năng tạo thành các hợp chất ổn định với hầu hết mọi nguyên tố, ngoại trừ các khí trơ.
-
Nóng chảy: Lưu huỳnh nóng chảy thường có độ nhớt, đây cũng là tính chất nổi bật của phi kim này. Độ nhớt của lưu huỳnh tăng lên theo nhiệt độ do sự hình thành các chuỗi polyme.
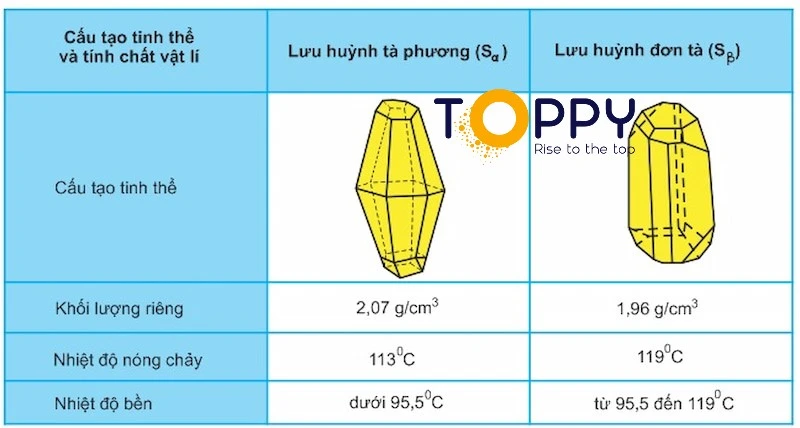
Dạng hình thù của lưu huỳnh
Lưu huỳnh có hai dạng thù hình, là lưu huỳnh tà phương Sα và lưu huỳnh đơn tà Sβ. Hai dạng thù hình này khác nhau về cấu tạo tinh thể và một số tính chất vật lí, nhưng lại mang tính chất hóa học giống nhau. Hai dạng lưu huỳnh Sα và Sβ này có thể biến đổi qua lại với nhau tùy theo điều kiện nhiệt độ. Theo dõi bảng dưới đây để hiểu chi tiết sự biến đổi qua lại này:
Ảnh hưởng của nhiệt độ đến tính chất vật lý của lưu huỳnh
Tính chất vật lý của lưu huỳnh có sự biến đổi rõ rệt theo nhiệt độ khác nhau. Cụ thể là:
-
Ở nhiệt độ dưới 113 độ: Sα và Sβ đều là chất rắn màu vàng. Trong phân tử có 8 nguyên tử liên kết cộng hóa trị với nhau tạo mạch vòng.
-
Ở nhiệt độ 119 độ: Sα và Sβ nóng chảy thành chất lỏng màu vàng và rất linh động.
-
Ở nhiệt độ 187 độ: Lưu huỳnh lỏng ở trạng thái quánh nhớt và có màu nâu đỏ.
-
Ở nhiệt độ 445 độ: Lưu huỳnh sôi, các phân tử lưu huỳnh bị phá vỡ thành nhiều phân tử nhỏ bay hơi.
3. Tính chất hóa học của lưu huỳnh
Điểm nổi bật trong tính chất hóa học của lưu hình là nó vừa thể hiện tính oxi hóa với các mức oxi hóa khác nhau, bao gồm: -2, 0, +4, +6, lại vừa thể hiện tính khử. Cùng tìm hiểu chi tiết tính chất này trong các thí nghiệm lưu huỳnh tác dụng với kim loại, Hidro và phi kim.
Tác dụng với hidro
Khi dẫn khí H2 vào ống thí nghiệm đựng lưu huỳnh đang sôi, lưu huỳnh phản ứng trực tiếp với Hidro. Quan sát thí nghiệm, ta nhận thấy có khí mùi trứng thối xuất hiện, đó là hiđro sunfua.
Phương trình phản ứng: H2 + S →H2S (điều kiện nhiệt độ: 350 độ)
Tác dụng với kim loại
Tác dụng với kim loại là một trong những tính chất hóa học đặc trưng của lưu huỳnh. Khi đun nóng, lưu huỳnh có khả năng tác dụng với nhiều kim loại tạo ra nhiều hợp chất khác nhau.
Ví dụ:
-
Khi trộn hỗn hợp bột sắt và lưu huỳnh, sau đó đun nhẹ. Quan sát phản ứng, ta thấy phản ứng tỏa nhiều nhiệt và xảy ra mạnh hơn theo phương trình: FE + S → FeS (điều kiện nhiệt độ)
-
Lưu huỳnh tác dụng với kẽm và nhôm cũng xảy ra phản ứng mạnh kèm theo sự lóe sáng. Những sợi đồng mảnh có thể cháy trong lưu huỳnh tạo ra CuS có màu đen.
Tác dụng với phi kim
Ở nhiệt độ thường, lưu huỳnh tác dụng với hầu hết các nguyên tố phi kim mạnh hơn như flo, oxi, clo… trừ iot và nitơ. Khi đốt cháy lưu huỳnh trong trong không khí ta được lưu huỳnh (IV) oxit với ngọn lửa màu xanh.
S + O2 → SO2 (nhiệt độ)
S + 3F2 → SF6 (nhiệt độ)
4. Điều chế lưu huỳnh như thế nào? So2 ra S
Ở phần này, chúng ta cùng tìm hiểu hai cách điều chế lưu huỳnh theo hai phương pháp phổ biến hiện nay: Trong phòng thí nghiệm và điều chế trong công nghiệp.
Trong phòng thí nghiệm
Trong phòng thí nghiệm, lưu huỳnh được điều chế bằng cách: Cho muối sunfit (muối của axit yếu) tác dụng với axit mạnh hơn (thường là dung dịch axit sunfuric với muối natri sunfit) theo quy trình sau:
-
Rót từ từ dung dịch axit sunfuric vào bình có chứa natri sunfit, sau đó đậy nắp lại theo phương trình: H2SO4 + Na2SO3 → Na2SO4 + SO2 + H2O (điều kiện: đun nóng). Chú ý cần để bình thu khí dựng thẳng, vì SO2 nặng hơn không khí.
-
Đun nóng bình trên ngọn lửa đèn cồn và sử dụng lưới amiang. Loại lưới này có tác dụng chống không cho ngọn lửa tập trung tại một chỗ và làm vỡ bình khi đun nóng dung dịch
Trong công nghiệp
Trong công nghiệp, lưu huỳnh được điều chế bằng những phương pháp phổ biến sau:
-
Đốt lưu huỳnh: S + O2 (nhiệt độ) → SO2
-
Đốt cháy H2S trong oxi dư: 2H2S + 3O2 → 2H2O + 2SO2
-
Cho kim loại tác dụng với H2SO4 (đặc nóng):
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
-
Đốt quặng pirit sắt (FeS2): 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
5. Những ứng dụng quan trọng của So2 ra S trong công nghiệp và đời sống
Lưu huỳnh là một trong những nguyên tố liên quan đến nhiều lĩnh vực trong đời sống thực tiễn, góp vai trò quan trọng trong nền kinh tế thế giới.
Ứng dụng của lưu huỳnh trong công nghiệp
Trong công nghiệp, 90% lượng lưu huỳnh được khai thác thông qua dẫn xuất chính là axít sulfuric (H2SO4), đây được đánh giá là một trong các nguyên tố quan trọng nhất được sử dụng như một nguyên liệu công nghiệp. Việc tiêu thụ acid sulfuric còn được coi là một trong các chỉ số tốt nhất về sự phát triển công nghiệp của một quốc gia. Lưu huỳnh được sản xuất ở Hoa Kỳ hàng năm nhiều hơn bất kỳ hóa chất công nghiệp nào khác.
Lưu huỳnh được sử dụng trong nhiều sản phẩm công nghiệp, ví dụ như: Ắc quy, bột giặt, lưu hóa cao su, thuốc diệt nấm và các phân bón photphat.
Ứng dụng của lưu huỳnh trong làm đẹp
Từ xa xưa, con người đã biết ứng dụng lưu huỳnh trong việc làm đẹp da và trị mụn trứng cá. Tuy nhiên, hiện nay vẫn chưa có nghiên cứu rõ ràng nào tìm ra cách hoạt động của nguyên tố này trong việc điều trị mụn.
Qua thực nghiệm, người ta đưa ra kết luận: Lưu huỳnh có khả năng kháng viêm và kháng khuẩn cao, từ đó có khả năng khiến những nốt mụn xẹp đi một cách nhanh chóng.

Bài tập vận dụng liên quan So2 ra S
Câu 1. Cho phản ứng: SO2 + 2H2S → 3S + 2H2O. Câu nào diễn tả đúng tính chất của các chất?
A. SO2 bị oxi hóa và H2S bị khử.
B. SO2 bị khử và H2S bị oxi hóa.
C. SO2 khử H2S và không có chất nào bị oxi hóa.
D. SO2 bị khử, lưu huỳnh bị oxi hóa.
Câu 2. Để nhận biết SO2 và SO3 người ta dùng thuốc thử:
A. Nước Clo
B. Nước vôi trong
C. Dung dịch Brom
D. Tất cả đều không được
Câu 3. Để oxi hóa cùng một số mol H2S theo các phản ứng dưới đây (chưa cân bằng) thì trường hợp nào khối lượng chất oxi hóa cần dùng là lớn nhất?
A. H2S + O2 → S +H2O
B. H2S + K2Cr2O7 + H2SO4 → S + Cr2(SO4)3 + K2SO4 + H2O
C. H2S + Cl2 + H2O → H2SO4 + HCl
D. H2S + SO2 → S + H2O
Câu 4. Trường hợp nào sau đây không xảy ra phản ứng hóa học?
A. 3O2 + 2H2S → 2H2O + 2SO2
B. FeCl2 + H2S → FeS + 2HCl
C. SO2 + 2H2S → 3S + 2H2O
D. SO3 + 2NaOH → Na2SO4 + H2O
Câu 5. Cho V (lít) SO2 (đktc) hấp thụ hoàn toàn vào 100ml dung dịch NaOH 2M thu được hỗn hợp 2 muối có khối lượng là 16,7g
A. 3,36 lit
B. 1,87 lit
C. 4,48 lit
D. 1,12 lit
Đáp án APhương trình hóa học
NaOH + SO2 → NaHSO3
NaOH + 2SO2 → Na2SO3 + H2O
Gọi x, y lần lượt số mol của 2 muối NaHSO3, Na2SO3
Bảo toàn nguyên tố Na có nNaHSO3 + 2.nNa2SO3 = nNaOH => x + 2y = 0,2
mNaHSO3 + mNa2SO3 = 16,7 <=> 104x + 126y = 16,7
=> x = 0,1; y = 0,05
Bảo toàn nguyên tố S có: nSO2 = nNaHSO3 + nNa2SO3 = x + y = 0,1 + 0,05 = 0,15
=> V = 0,15.22,4 = 3,36 lit
Câu 6. Thực hiện thí nghiệm sau: cho khí H2S lội qua dung dịch CuSO4 thấy có kết tủa màu xám đen xuất hiện, chứng tỏ:
A. Sau phản ứng có kết tủa trắng tạo thành
B. Có kết tủa CuS tạo thành, không tan trong axit mạnh
C. Axit sunfuric mạnh hơn axit sunfuahidric
D. Axit sunfuahidric mạnh hơn axit sunfuaric
Câu 7. Để điều chế khí H2S người ta sử dụng hóa chất, phản ứng nào sau đây
A. Mg tác dụng với H2SO4 không quá đặc
B. FeS tác dụng với dung dịch HCl loãng
C. FeS tác dụng với dung dịch H2SO4 đặc
D. S tác dụng với H2
Câu 8. Trộn 400 ml dung dịch NaOH 1M với 300ml dung dich H2SO4 1M. Hỏi sau khi phản ứng kết thúc khôi lượng muối thu được là bao nhiêu?
A. 19,1 gam
B. 9,55 gam
C. 38, 2 gam
D. 6,7 gam
Đáp án C
Ta có: nNaOH = 0,4 .1 = 0,4 (mol); nH2SO4 = 0,3 mol
Phương trình phản ứng
NaOH + H2SO4 → NaHSO4 + H2O
(mol) 0,3 ← 0,3 → 0,3
NaOH + NaHSO4 → Na2SO4 + H2O
(mol) 0,1 → 0,1
⇒ nNaHSO4 dư = 0,3 – 0,1 = 0,2 (mol)
⇒ mmuối = mNaHSO4 + mNaSO4 = 120.0,2 + 142 .0,1= 38,2 gam
Câu 9. Khi pha loãng H2SO4 đặc thực hiện thao tác nào sau đây đúng:
A. Cho từ từ H2SO4 đặc vào nước và khuấy đều
B. Cho từ từ nước vào H2SO4 đặc và khuấy đều
C. Cho nước và axit đồng thời vào cốc khuấy đều
D. Cho nhanh H2SO4 đặc vào nước và khuấy đều
Trên là thông tin về phương trình phản ứng So2 ra S và các bài tập có liên quan. Hy vong bài viết sẽ cung cấp thêm nhiều thông tin cho các bạn. Nếu có thắc mắc hãy mình luận bên dưới nhé.
…………………………….
Mời các bạn tham khảo thêm tài liệu liên quan