CH3cooc2h5 ra CH3coona | CH3COOC2H5 + NaOH → C2H5OH + CH3COONa

Ch3COOC2H5 ra CH3COONa là phản ứng chuyển hóa hóa học đáng chú ý trong lĩnh vực hóa học hữu cơ. Quá trình này tạo thành muối sodium acetate từ ethyl acetate và được sử dụng trong nhiều ứng dụng khác nhau. Từ công nghiệp, dược phẩm, cho đến ngành thực phẩm, sự tương tác này đóng vai trò quan trọng trong việc sản xuất và chế biến. Hãy cùng tìm hiểu thêm về quá trình chuyển hóa này và ứng dụng đa dạng mà nó mang lại cho cuộc sống hàng ngày của chúng ta.
Lý thuyết về Ch3COOC2H5 ra CH3COONa
Phương trình CH3COOC2H5 tác dụng với NaOH
CH3COOC2H5 + NaOH → C2H5OH + CH3COONa
Điều kiện phương trình phản ứng CH3COOC2H5 tác dụng với NaOH
Đun sôi nhẹ.
Cách thực hiện phản ứng CH3COOC2H5 tác dụng với NaOH
Cho 2ml etyl axetat vào ống nghiệm, sau đó cho tiếp dung dịch 1 ml NaOH 30%. Lắc đều ống nghiệm rồi đun cách thủy trong 5 phút.
Hiện tượng nhận biết phản ứng
Ban đầu chất lỏng trong ống nghiệm tách thành hai lớp. Sau phản ứng chất lỏng trong ống nghiệm trở thành đồng nhất.
Tính chất hóa học este
Phản ứng thủy phân môi trường Axit (H+)
R-COO-R’ + H-OH ⇋ R-COOH + R’-OH
Phản ứng thủy phân môi trường Bazơ (OH–)
R-COO-R’ + NaOH ⟶ R-COONa + R’-OH
Ví dụ:
CH3COOC2H5 + NaOH ⟶ CH3COONa + C2H5OH
CH2=CH-COO-CH3 + NaOH ⟶ CH2=CH-COONa + CH3-OH
Một số phản ứng Este đặc biệt
Este X + NaOH ⟶ 2 muối + H2O
⇒ X là este của phenol, có công thức là C6H5OOC–R
Este X + NaOH ⟶ 1 muối + 1 anđehit
⇒ X là este đơn chức, có công thức là R–COO–CH=CH–R’
Este X + NaOH ⟶ 1 muối + 1 xeton
⇒ X là este đơn chức, có công thức là R’–COO–C(R)=C(R”)R’’’
Este X + AgNO3/NH3 + H2O ⟶ 2Ag + 2 muối
⇒ X là este của axit focmic, có công thức là HCOO-R’
Phản ứng Este chứa gốc không no
- Phản ứng H2 (xt, Ni, to)
CH2=CH-COO-CH3 + H2 ⟶ C2H5COO-CH3
- Phản ứng trùng hợp (tạo polime)
nCH3COOCH=CH2 ⟶ Poli (vinyl axetat)
nCH2=C(CH3)-COOCH3 ⟶ Thủy tinh hữu cơ.
Nội dung mở rộng về CH3COOC2H5
Định nghĩa
- Định nghĩa: Etyl axetat là một este với công thức CH3COOC2H5
- Công thức phân tử: C4H8O2
- Công thức cấu tạo: CH3COOC2H5
- Tên gọi
- Tên gốc chức: Etyl axetat
- Danh pháp quốc tế: Etyl etanonat
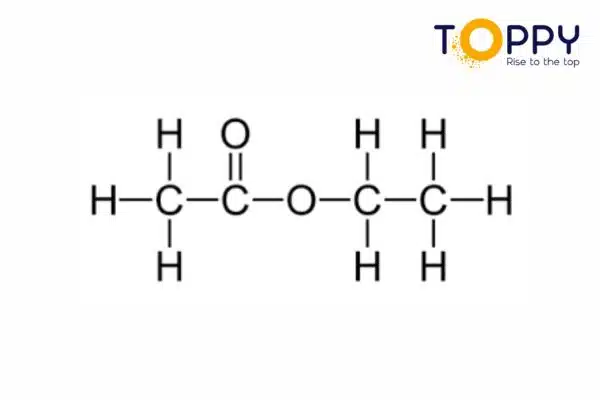
Cấu tạo của Etyl axetat
Etyl Axetat (CH3COOC2H5) có những tính chất vật lý nào?
Etyl Axetat (CH3COOC2H5) được biết đến là một chất lỏng ở điều kiện thường, có mùi thơm ngọt đặc trưng, mùi này gần giống như mùi sử dụng trong chất sơn móng tay.
Ở dạng lỏng nó là một dung môi phân cực nhẹ, tương đối không gây ra độc hại cho con người, dễ dàng bay hơi và không hút ẩm. Khi hòa Etyl Axetat (CH3COOC2H5) vào nước, nó có thể tan được tối đa 8%. Nhiệt độ càng tăng thì khả năng nó hòa tan trong nước càng lớn hơn.
Etyl Axetat (CH3COOC2H5) tan nhiều trong các dung môi hữu cơ như: etanol, axeton, benzen, dietyl ete. Trong môi trường axit hay bazơ mạnh, Etyl Axetat có tính không ổn định.
Tính chất hóa học
- Phản ứng thủy phân trong môi trường axit
- Phản ứng thủy phân trong môi trường kiềm
- Phản ứng đốt cháy: Phản ứng oxi hóa hoàn toàn tạo CO2 và H2O
CH3COOC2H5 + 5O2 → 4CO2 + 4H2O
Cách điều chế Etyl Axetat trong phòng thí nghiệm
Etyl Axetat (CH3COOC2H5) được điều chế thông qua phản ứng este hóa. Đây là cách điều chế etyl axetat trong phòng thí nghiệm nhanh gọn nhất. Chúng ta sẽ cho Axit Axetic tác dụng với Etanol trong điều kiện nhiệt độ và Axit Sunfuric làm chất xúc tác.
Phương trình điều chế Etyl Axetat (CH3COOC2H5):
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
Dụng cụ cần chuẩn bị: Đèn cồn, ống nghiệm, kẹp gỗ, các loại hóa chất,…
Cách làm: Cho Ancol Etylic, Axetic nguyên chất với tỉ lệ bằng nhau vào ống nghiệm. Tiếp theo nhỏ vào một giọt axit sunfuric đặc. Tiến hành lắc đều ống và đun cách thủy 5 – 6 phút (đun trên lửa đèn cồn cũng được). Sau đó tiến hành làm lạnh nhanh, rót thêm một ít NaCl bão hòa vào thì thấy dung dịch đã tách lớp và có mùi thơm đặc trưng. Este không tan sẽ nằm ở trên lớp nước.
Tính chất về Etyl axetat
Ứng dụng
- Etyl axetat được dùng rộng rãi làm dung môi cho các phản ứng hóa học cũng như để thực hiện công việc chiết các hóa chất khác.
- Tương tự, nó cũng được dùng trong sơn móng tay và thuốc tẩy sơn móng tay hay dùng để khử cafein của các hạt cà phê.
- Etyl axetat cũng có mặt trong một số loại kẹo, hoa quả hay nước hoa do nó bay hơi rất nhanh và để lại mùi nước hoa trên da. Nó cũng tạo ra hương vị tương tự như của các loại quả đào, mâm xôi.
- Etyl axetat còn là một chất độc có hiệu lực để sử dụng trong thu thập và nghiên cứu côn trùng.
Bài tập trắc nghiệm liên quan
Câu 1. Este etyl axetat có công thức là
- CH3COOCH3
- CH3COOC2H5.
- CH3CH2OH.
- CH3COOC3H7
Đáp án B
Etyl axetat có công thức cấu tạo là CH3COOC2H5
Câu 2. Thủy phân vinyl axetat trong dung dịch KOH thu được:
- axit axetic và ancol vinylic
- kali axetat và ancol vinylic
- kali axetat và anđehit axetic
- axit axetic và anđehit axetic
Đáp án C
vinyl axetat có công thức hóa học là: CH3COOCH=CH2
Phương trình phản ứng thủy phân vinyl axetat
CH3COOCH=CH2 + KOH → CH3COOK + CH3-CH=O
Câu 3. Cho các nhận định sau:
(a). Chất béo là trieste của glixerol với các axit monocacboxylic có mạch C dài không phân nhánh.
(b). Lipit gồm các chất béo, sáp, steroid, photpholipit,…
(c). Chất béo là chất lỏng, không màu
(d). Chất béo chứa các gốc axit không no thường là chất lỏng ở nhiệt độ thường và được gọi là dầu.
(e). Phản ứng thủy phân chất béo trong môi trường kiềm là phản ứng thuận nghịch.
(g). Chất béo là thành phần chính của dầu mỡ động vật và thực vật.
Các nhận định nào trên đúng là:
- (b), (d); (g)
- (a), (c); (e),
- (a), (c); (e), (g)
- (b), (c); (d); (e), (g)
Đáp án A. (b), (d); (g)
(a) . Sai, vì chất béo là trieste của axit monocacboxylic có số C chẵn từ 12-24, không phân nhánh
(c). Sai, vì chất béo no là chất rắn
(e). Sai, vì phản ứng thủy phân chất béo trong môi trường kiềm là phản ứng 1 chiều
Câu 4: Cho 20 gam một este X (có phân tử khối là 100đvc) tác dụng với 300 ml dung dịch NaOH 1M.
Sau phản ứng, cô cạn dung dịch thu được 23,2g chất rắn khan. Công thức cấu tạo thu gọn của X là
- CH2=CHCH2COOCH3.
- CH3COOCH=CHCH3.
- C2H5COOCH=CH2.
- CH2=CHCOOC2H5.
Đáp án C
nX = 20/100 = 0,2 mol;
nNaOH = 1.0,3 = 0,3 mol
Số mol nNaOH dư = 0,3 – 0,2 = 0,1 mol.
m chất rắn sau phản ứng = mmuối + mNaOH dư
Khối lượng muối thu được: mmuối = 23,2 – 0,1.40 = 19,2 gam
Mmuối = 19,2/0,2 = 96
Muối là C2H5COONa
Este X cần tìm là: C2H5COOCH=CH2
Câu 5: Thuỷ phân hoàn toàn 444 gam một lipit X thu được 46 gam glixerol và hai loại axit béo. Hai loại axit béo đó là
- C17H31COOH và C17H33COOH.
- C15H31COOH và C17H35COOH.
- C17H33COOH và C15H31COOH.
- C17H33COOH và C17H35COOH.
Đáp án D
Phản ứng thủy phân tạo 2 muối
Phương trình hóa học dạng tổng quát
(R1COO)2C3H5(OOCR2) + 3NaOH → 2R1COONa + R2COONa + C3H5(OH)3
nlipit = nglixerol → nlipit = 46/92 = 0,5mol
→Mlipit = 444/0,5 = 888 g/mol
→ (R1 + 44).2 + (R2 + 44) + 41 = 888 → 2R1 + R2 = 715
R1 = 239 (C17H35)
R2 = 237 (C17H33)
→ C17H33COOH và C17H35COOH.
Câu 6: Hóa hơi 27,2 gam một este X thu được 4,48 lít khí (quy về đktc).
Xà phòng hóa X bằng dung dịch NaOH (vừa đủ) thu được hỗn hợp hai muối của natri. Công thức cấu tạo thu gọn của este X là
- CH3COOC6H5.
- C6H5COOCH3.
- CH3COOC6H4CH3.
- HCOOC6H5.
Đáp án B
neste = 0,2 mol => Meste = 27,2/0,2 = 136
X + NaOH → 2 muối => X là este của phenol
Do đó, X có dạng C6H5OOCR => 121 + R = 136 => R = 15
Vậy X là C6H5OOCCH3
Câu 7: Trùng hợp m tấn etilen thu được 1 tấn polietilen (PE) với hiệu suất phản ứng bằng 80%. Giá trị của m là
A.1,25
- 0,80
- 1,80
- 2,00
Câu 8: Ba hiđrocacbon X, Y, Z kế tiếp nhau trong dãy đồng đẳng, trong đó khối lượng phân tử Z gấp đôi khối lượng phân tử X.
Đốt cháy 0,1 mol chất Y,sản phẩm khi hấp thụ hoàn toàn vào dung dịch Ca(OH)2 dư, thu được số gam kết tủa là
- 30 gam
- 10gam
- 40 gam
- 20 gam
Đáp án C
Gọi MX là phân tử của X.
Phân tử khối của Z = MX + 28 = 2 MX
=> MX = 28, X là C2H4.
=> Y là C3H6 và Z là C4H8.
0,1 mol Z khi đốt thu 0,4 mol CO2 và khi hấp thụ vào Ca(OH)2 dư thu 0,4 mol CaCO3 nặng 40 gam.
…………………………………
Tổng kết lại, quá trình Ch3COOC2H5 ra CH3COONa đóng vai trò quan trọng trong lĩnh vực hóa học hữu cơ và có ứng dụng đa dạng trong cuộc sống hàng ngày. Sự chuyển hóa này tạo ra muối sodium acetate từ ethyl acetate và được áp dụng rộng rãi trong công nghiệp, ngành dược phẩm. Từ việc sử dụng làm chất bảo quản trong thực phẩm đến ứng dụng trong sản xuất hóa chất, quá trình này đã chứng tỏ tính hiệu quả và hữu ích. Đồng thời, việc nghiên cứu quá trình Ch3COOC2H5 ra CH3COONa có thể đóng góp vào việc bảo vệ môi trường và phát triển bền vững cho xã hội.
Xem thêm: