C6h12o6 ra c2h5oh | Phương trình C6H12O6 → C2H5OH + CO2

C6H12O6 → C2H5OH + CO2 được Toppy biên soạn cũng là phương trình hóa học điều chế rượu etyllic trong điều kiện thích hợp glucozơ lên men tạo thành khí CO2 và glucozo ra ancol etylic. Hy vọng giúp các bạn viết và cân bằng đúng phương trình. Đây là một phương trình khó nên các em hãy tập trung để hiểu sâu hơn nhé.
Phương trình C6h12o6 ra c2h5oh
Phương trình phản ứng C6h12o6 ra c2h5oh
C6H12O6 → 2C2H5OH + 2CO2
Điều kiện phản ứng C6h12o6 ra c2h5oh
Nhiệt độ: 30 – 35°C Xúc tác: enzim
Nội dung mở rộng của phương trình C6h12o6 ra c2h5oh
Định nghĩa Ethanol là gì?
Ethanol (etanol) còn có tên gọi khác là rượu etylic, rượu ngũ cốc, ancol etylic hay phổ biến nhất là cồn. Đây là một chất lỏng không màu, dễ bay hơi, tan vô hạn trong nước. Nó còn được gọi phổ biến là rượu.
Công thức hóa học của cồn là C2H5OH, chúng được sản xuất dựa vào quá trình lên men các nguồn hydratcacbon có sẵn trong tự nhiên như lúa mì, đường, lúa mạch, ngô, sắn, mùn, gỗ. Trong công nghệ tổng hợp hóa dầu, ethanol được điều chế theo dây chuyền công nghệ hydrat hóa khí etylen bằng chất xúc tác acid.
C2H5OH là gì?
Ethanol được chia làm hai loại cồn công nghiệp và cồn thực phẩm. Mỗi loại mang những đặc điểm, tính chất nồng độ thành phần và tạp chất khác nhau nhưng chúng có tính chất vật lý đặc trưng:
- Mùi đặc trưng như rượu
- Nếu không bảo quản tốt rất dễ bay hơi
- Chất lỏng không màu, trong suốt
- Tỷ trọng : 0,799 ÷ 0,8 (so với nước)
- Tan vô hạn trong nước
- Nhiệt độ sôi: -117,3oC
- Có tính hút ẩm mạnh
Quy trình điều chế C2H5OH với phương trình C6h12o6 ra c2h5oh
Ví dụ về quy trình nấu rượu gạo công nghiệp
Cồn thực phẩm và cồn công nghiệp được sản xuất theo quy trình lên men từ khoai, ngũ cốc, mía, gạo… với nồng đổ 96 – 99% theo các bước sau đây:
- Nấu nguyên liệu: Tinh bột sẽ được nấu, sau một thời gian sẽ trương nở và hồ hóa rồi nguội về nhiệt độ thích hợp để thực hiện cho bước tiếp theo.
- Đường hóa nguyên liệu: Có hai phương pháp để thực hiện đó là đường hóa bằng chế phẩm Amylase của nấm mốc và đường hóa bằng acid.
- Lên men dịch đường: Bước này có thể sử dụng hai phương pháp, lên men gián đoạn và lên men liên tục.
- Chưng cất và tinh chế: Chưng cất giúp tách các tạp chất dễ bay hơi và cồn ra khỏi dấm chín để thu được cồn thô.
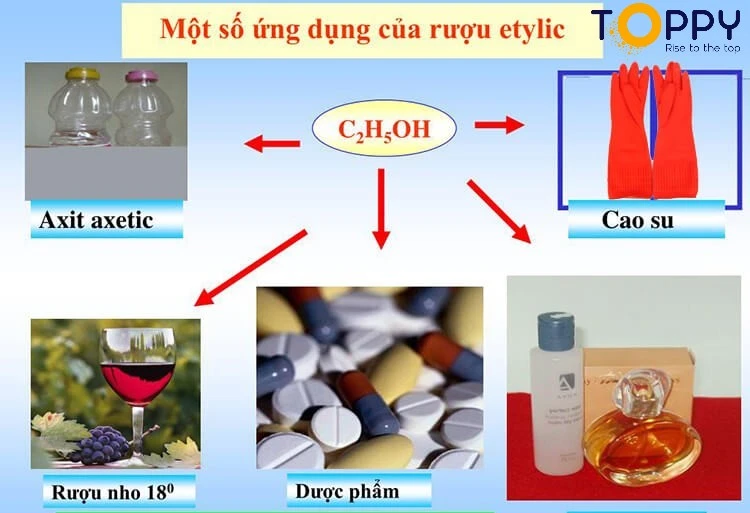
Ứng dụng của cồn ethanol C2H5OH và phương trình C6h12o6 ra c2h5oh
Ứng dụng của C2H5OH trong công nghiệp và đời sống
Trong công nghiệp
- Phần lớn lượng cồn ethanol C2H5OH được sản xuất ra được dùng làm dung môi trong ngành công nghiệp dược phẩm, nước hóa, dệt may, in ấn, sơn,… Đồng thời nó còn là một dung môi hoàn hảo giúp hòa tan các chất, ngăn ngừa được sự kết tinh của các thành phần trong mỹ phẩm.
- C2H5OH được dùng như là nhiên liệu cồn và các hàng loạt các quy trình công nghiệp khác. Đặc biệt, nó còn được sử dụng trong các sản phẩm chống đông lạnh. Etanol còn được dùng làm nhiên liệu đốt cho đèn cồn phòng thí nghiệm, dùng thay xăng làm nhiên liệu cho động cơ đốt trong.
- Cồn công nghiệp còn được dùng làm nguyên liệu để sản xuất các hợp chất hữu cơ khác như ete, axit axetic,… nó còn là nguyên liệu hóa học đa dụng.
Trong ngành y tế
- Ethanol được sử dụng chống vi khuẩn, vi sinh vật trong y tế.
- Với khả năng gây mê, gây buồn ngủ nên C2H5OH còn được sử dngj sản xuất thuốc ngủ.
- Với đặc tính sát khuẩn cao, Etanol 70 – 90% được dùng để khử trùng các thiết bị, dụng cụ, vết thương,… Đem lại hiệu quả chống lại các vi khuẩn gây nấm cũng như những loại virus khác.
Trong thực phẩm
- Cồn thực phẩm được ứng dụng trong sản xuất nấu rượu, ướp gia vị, pha chế thuốc, sát trùng, đồ uống có cồn, mỹ phẩm,..
- Dùng trong bảo quản thực phẩm. Ngoài ra, ethanol còn là thành phần chủ yếu trong các loại nước hoa cao cấp và nước xịt phòng.
Ethanol trong mỹ phẩm
Cồn ethanol có trong mỹ phẩm giúp dưỡng da hoặc sử dụng làm dung môi bao gồm 2 loại:
- Cồn béo (tiếng anh là Fatty Alcohol) hay còn được gọi là cồn tốt giúp cân bằng độ ẩm cũng như giúp da mềm mịn hơn và không gây kích ứng da. Tuy nhiên, cồn béo lại dễ gây tắc, bí lỗ chân lông trên da nên không được khuyến khích với những người có da mụn, da dầu.
- Cồn khô (tiếng anh Drying Alcohols) hay còn gọi là cồn xấu với khả năng khử trùng, chống khuẩn. Cồn khô tốt cho da nhờn vì giúp hạn chế tiết dầu, giúp da sạch, không bị bí lỗ chân lông.
Mỗi loại cồn ethanol đều có những thế mạnh riêng nên chúng là thành phần của nhiều loại mỹ phẩm, xuất hiện trong nhiều công thức dưỡng da, làm đẹp.
Ethanol có độc không?
Etanol (rượu) khi được đưa vào cơ thể sẽ chuyển hóa thành axêtalđêhít hay Formaldehyd mà đây là chất có độc tính cao hơn etanol. Rượu là nguyên nhân của rất nhiều căn bệnh nguy hiểm như: ung thư, bệnh xơ gan mà đặc biệt là chứng nghiện rượu
Dù không có độc tính cao nhưng etanol có thể gây tử vong khi nồng độ cồn trong máu ở ngưỡng 0,4% – 0,5% hoặc cao hơn. Etanol có trong máu ở nồng độ 0,3% – 0,4% gây ra tình trạng hôn mê.
Các nghiên cứu đã chỉ ra rằng, etanol và Acinetobacter baumannii (vi khuẩn gây bệnh viêm màn não, viêm phổi,…) có mối quan hệ tỉ lệ thuận với nhau.

Etanol có thể gây tử vong nếu uống quá liều lượng
Lưu ý khi sử dụng ethanol và sự hiểu biết về phương trình C6H12O6 → C2H5OH + CO2
- Các hỗn hợp etanol 50 độ trở lên là các chất dễ cháy và dễ dàng bắt lửa nên cần phải bảo quản ở nơi thống gió, tránh xa ánh nắng mặt trời, tránh xác bình xịt, các nguyên tố dễ cháy, chất ăn mòn.
- Khi tiếp xúc với cồn công nghiệp cần đeo khẩu trang và đồ dùng bảo hộ theo quy định.
- Tuyệt đối không pha cồn công nghiệp để uống.
- Khi có chát cần dùng bột, bọt CO2 hoặc hóa chất khô để xử lý. Tuyệt đối không dùng nước.
Etanol dễ cháy khi gặp lửa
Sự khác nhau giữa Methanol và Ethanol
Đây là hai loại dung môi công nghiệp được sử dụng phổ biến hiện này. Đều được gọi là cồn nhưng quá trình sản xuất và đặc điểm lại khác nhau, cụ thể như:
- Ethanol được sản xuất từ tinh bột, các loại ngũ cốc. Cồn methanol được sản xuất từ các vật liệu có chứa Cenlulose.
- Metanol độc hơn Ethanol, có thể gây mù, đau đầu, buồn nôn thậm chí tử vong khi nuốt phải.
- Rượu Methanol thường có bọt khi lật ngược chai lại, Rượu Etanol không có bọt.
- Cho một lượng nhỏ dung dịch vào tay, khi cọ sát C2H5OH hơi dính còn CH3OH sẽ bốc hơi nhanh.
Ethanol khác với Methanol
Bài tập vận dụng liên quan đến phương trình C6h12o6 ra c2h5oh
Câu 1. Để sản xuất glucozo trong công nghiệp, người ta sử dụng phương pháp nào sau đây:
A. đi từ tinh bột bằng phản ứng thủy phân
B. lấy từ nguồn mật ong rừng có trong tự nhiên
C. từ một số loại quả chín chứa nhiều glucozo
D. từ đường saccarozo bằng phản ứng thủy phân
Câu 2. Cho 50 ml dd glucozơ chưa rõ nồng độ tác dụng với một lượng dư AgNO3 trong dd NH3 thu được 1,08 gam Ag kết tủa. Nồng độ mol/l của dung dịch glucozơ đã dùng là:
A. 0,2M
B. 0,01M.
C. 0,10M.
D. 0,02M.
Đáp án CnAg = 1,08/108 = 0,01 (mol)
C6H12O6 → 2Ag
0,02 (mol) ← 0,01 (mol)
Vì n(C6H12O6) = 1/2nAg = 1/2.0,01 = 0,005 (mol)
⇒CM(C6H12O6) = 0,005/0,05 = 0,1M
Câu 3. Cho a gam glucozơ phản ứng với dung dịch AgNO3/NH3 tạo thành a gam Ag. Phần trăm của glucozơ tham gia phản ứng là
A. 83,33%,
B. 41,66%.
C. 75,00%.
D. 37,50%.
Câu 4. Phát biểu nào sau đây không đúng?
A. Glucozơ tác dụng được với nước brom.
B. Khi glucozơ tác dụng với CH3COOH (dư) cho este 5 chức.
C. Glucozơ tồn tại ở dạng mạch hở và dạng mạch vòng.
D. Ở dạng mạch hở, glucozơ có 5 nhóm OH kề nhau.
Câu 5. Trong chế tạo ruột phích người ta thường dùng phương pháp nào sau đây:
A. Cho axetilen tác dụng với dung dịch AgNO3/NH3
B. Cho anđehit fomic tác dụng với dung dịch AgNO3/NH3
C. Cho axit fomic tác dụng với dung dịch AgNO3/NH3
D. Cho glucozơ tác dụng với dung dịch AgNO3/NH3
Câu 6. Cho 360 gam glucozơ lên men tạo thành ancol etylic, khí sinh ra được dẫn vào dung dịch nước vôi trong dư thu được m gam kết tủa. Biết hiệu suất của quá trình lên men đạt 80 %. Vậy giá trị của m là:
A. 200 gam
B. 320 gam
C. 400 gam
D. 160 gam
Đáp án BTa có:
Glu = 360:180 = 2 (mol)
Vì H = 80% nên số mol Glu thực tế tham gia phản ứng là: nGlu = 2. 80%:100% = 1,6 (mol)
C6H12O6 → 2CO2 →2CaCO3
1,6 → 3,2 (mol)
mCaCO3 = 3,2.100 = 320 (g)