HCOOH AgNO3 NH3 | HCOOH + AgNO3 + H2O + NH3 → (NH4)2CO3 + Ag + NH4NO3

Phản ứng HCOOH AgNO3 NH3 là một quá trình hóa học đáng chú ý và có nhiều ứng dụng trong ngành công nghiệp và y học. Phản ứng này có thể được sử dụng trong tổng hợp hợp chất, phân tích hóa học và nghiên cứu y học. Nghiên cứu sâu hơn về phản ứng HCOOH AgNO3 NH3 sẽ giúp chúng ta hiểu rõ hơn về các ứng dụng tiềm năng và đóng góp tích cực cho phát triển công nghệ và y học.
Lý thuyết về HCOOH AGNO3 NH3
Điều kiện phản ứng HCOOH tác dụng với dung dịch AgNO3/NH3
Điều kiện: Không có
Cách tiến hành phản ứng cho HCOOH tác dụng với dung dịch AgNO3/NH3
Cho axit formic HCOOH tác dụng với AgNO3 trong dung dịch NH3
Hiện tượng hóa học
Axit fomic HCOOH tác dụng với AgNO3 trong dung dịch NH3 tạo ra kết tủa trắng bạc, hay còn gọi là phản ứng tráng gương.
Nội dung mở rộng về AgNO3
AgNO3 là gì?
AgNO3 là công thức hóa học của bạc nitrat. Đây là một hợp chất phổ biến của bạc với axit nitric, có nhiều tên gọi khác nhau như bạc đơn sắc, muối axit nitric (I), …
Hóa chất này được biết đến như một tinh thể không màu, dễ hòa tan trong nước. Dung dịch AgNO3 chứa một lượng lớn các ion bạc, chính vì vậy mà nó có đặc tính oxy hóa mạnh và có tính ăn mòn nhất định.
Đây là hóa chất được sử dụng phổ biến hiện nay để mạ bạc, phản chiếu, in ấn, trong y học, nhuộm tóc…
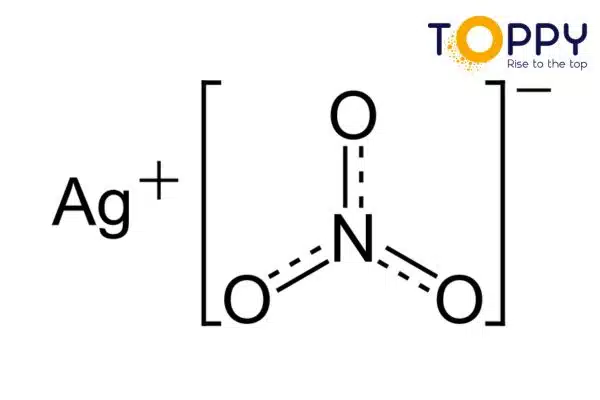
Cấu tạo phân tử của AgNO3 Bạc Nitrat
Cấu tạo phân tử của AgNO3 Bạc Nitrat
Những tính chất lí hóa của nitrat bạc
Tính chất vật lí của AgNO3 là gì?
- Là một tinh thể dễ vỡ, trong suốt không màu.
- Hòa tan trong nước và amoniac, ít tan trong ethanol khan, và gần như không hòa tan trong axit nitric đậm đặc.
- Dung dịch của nó có tính axit yếu, tính oxy hóa mạnh và có tính ăn mòn nhất định.
| KHỐI LƯỢNG RIÊNG | 5.35 g/cm3 |
| ĐIỂM NÓNG CHẢY | 212 °C (485 K; 414 °F) |
| ĐIỂM SÔI | 444 °C (717 K; 831 °F) |
| ĐỘ HÒA TAN TRONG NƯỚC | 1220 g/L (0 °C)
2160 g/L (20 °C) 4400 g/L (60 °C) 7330 g/L (100 °C) |
| ĐỘ HÒA TAN | hòa tan trong acetone, Amoniac, Ete, Glyxerol |
| CHIẾT SUẤT (ND) | 1.744 |
Những tính chất hóa học của AgNO3 là gì?
Sau đây là những tính chất hóa học nổi bật của bạc nitrat:
- Tham gia phản ứng oxi hóa khử:
N2H4 + 4AgNO3 → 4Ag + N2 + 4HNO3
H3PO3 + 2AgNO3 + H2O → 2Ag + H3PO4 + 2HNO3
2AgNO3 + Cu → Cu(NO3)2 + 2Ag
- Tham gia phản ứng phân hủy:
AgNO3 → 2Ag + 2NO2 + O2
- Có phản ứng với NH3:
2AgNO3 + 2NH3 · H2O → Ag2O + H2O + 2NH4NO3 (lượng nhỏ amoniac)
AgNO3 + 3NH3 · H2O → Ag(NH3)2OH + NH4NO3 + 2H2O (amoniac dư)
- Tham gia phản ứng với axit:
AgNO3 + HCl → AgCl + HNO3
HBr + AgNO3 → AgBr + HNO3
- Phản ứng với NaOH:
2NaOH + 2AgNO3 → 2NaNO3 + Ag2O + H2O
- Phản ứng với khí clo:
Cl2 + H2O → HCl + HClO HCl + AgNO3 → AgCl + HNO3
Điều chế AgNO3 Bạc Nitrat ra sao?
Sau đây là một số cách giúp điều chế AgNO3:
- 3 Ag + 4 HNO3(lạnh và loãng) → 3 AgNO3 + 2 H2O + NO
- 3 Ag + 6 HNO3(đậm đặc, nóng) → 3 AgNO3 + 3 H2O + 3 NO2
(Lưu ý: Quá trình này cần điều kiện có tủ hút khí độc do chất độc nitơ ôxit sinh ra trong phản ứng vô cùng nguy hiểm).
Điều chế AgNO3 Bạc Nitrat ra sao
Những ứng dụng quan trọng của AgNO3 trong cuộc sống, sản xuất
- Bạc Nitrat được dùng để kết tửa các ion clorua.
- AgNO3 được sử dụng để hiệu chuẩn dung dịch natri clorua.
- Được sử dụng để sản xuất các muối bạc khác.
- AgNO3 được sử dụng để tạo ra chất kết dính dẫn điện, máy lọc khí mới, quần áo cân bằng áp suất mạ bạc hay gang tay để làm việc trực tiếp.
- Nó cũng là vật liệu nhạy sáng cho phim, phim x-quang và phim ảnh.
- Được sử dụng để mạ bạc các linh kiện điện tử và thủ công mỹ nghệ khác…
- AgNO3 được sử dụng trong sản xuất pin bạc – kẽm.
- AgNO3 có vai trò quan trọng trong y học, chúng giúp ăn mòn mô hạt tăng sinh và dung dịch loãng, sử dụng để làm thuốc diệt nấm trong chữa trị nhiễm trùng mắt.
- Hóa chất này là một tác nhân để phát hiện aldehyd và đường. Sử dụng để đo các ion clorua, chất xúc tác để xác định mangan, mạ điện, chụp ảnh và tô màu sứ.
Ứng dụng trong công nghiệp của AgNO3
Một số thông tin cần lưu ý về AgNO3
AgNO3 có độc hại hay không?
- AgNO3 là một chất rắn gây oxy hóa, nhóm 2, H272
- Chúng ăn mòm kim loại, nhóm 1, H290
- Ăn mòn da, Nhóm 1 B, H314
- Gây nguy hại cấp tính và mãn tính đối với môi trường thủy sinh
Những biện pháp xử lý khi tiếp xúc với AgNO3
- Nếu AgNO3 tiếp xúc với da: Cần phải cởi bỏ tất cả các quần áo bị nhiễm độc ngay, sau đó rửa sạch da bằng nước hoặc tắm ngay.
- Nếu hóa chất này tiếp xúc với mắt: Cần rửa sạch với nhiều nước.
- Nếu chẳng may nuốt phải hóa chất: Cần lập tức uống nước (không quá hai cốc) và hỏi ý kiến bác sĩ nếu cảm thấy không khỏe để được điều trị kịp thời.
Cần sơ cứu kịp thời khi AgNO3 tiếp xúc với mắt
Bài tập minh họa
Câu 1: Cho một lượng axit HCOOH tác dụng hoàn toàn với lượng dư dung dịch AgNO3/NH3 thu được 10,8 gam Ag. Tính lượng axit đã phản ứng
- 2,3 gam
- 4,6 gam
- 1,15 gam
- 9,2 gam
Câu 2: Chất nào dưới đây tham gia phản ứng tráng gương (tráng bạc):
- HCOOH
- CH3-O-CH3
- CH2=CH2
- C2H5OH
Câu 3: Công thức tổng quát của axit cacboxylic no, đơn chức, mạch hở là
- CnH2nO2.
- CnH2n+2O2.
- CnH2n+1O2.
- CnH2n-1O2.
Câu 4: Dùng hóa chất nào dưới đây để phân biệt axit fomic và axit axetat?
- CO2
- Quỳ tím
- NaOH
- Dung dịch AgNO3/NH3
Câu 5: Chất nào sau đây có thể làm khô khí NH3 có lẫn hơi nước?
- P2O5.
- H2SO4 đặc.
- CuO bột.
- NaOH rắn.
Câu 6: Tính bazơ của NH3 do
- trên N còn cặp e tự do.
- phân tử có 3 liên kết cộng hóa trị phân cực.
- NH3 tan được nhiều trong nước.
- NH3 tác dụng với nước tạo NH4OH.
Câu 7: Để tách riêng NH3 ra khỏi hỗn hợp gồm N2, H2, NH3 trong công nghiệp người ta đã
- Cho hỗn hợp qua nước vôi trong dư.
- Cho hỗn hợp qua bột CuO nung nóng.
- nén và làm lạnh hỗn hợp để hòa lỏng NH3.
- Cho hỗn hợp qua dung dịch H2SO4 đặc.
Câu 8: Chất nào sau đây có thể làm khô khí NH3 có lẫn hơi nước?
- P2O5.
- H2SO4 đặc.
- CuO bột.
- NaOH rắn.
Câu 9: Trong các phản ứng sau, phản ứng nào NH3 đóng vai trồ là chất oxi hóa?
- 2NH3 + H2O2 + MnSO4 → MnO2 + (NH4)2SO4
- 2NH3 + 3Cl2 → N2 + 6HCl
- 4NH3 + 5O2 → 4NO + 6H2O
- 2HN3 + 2Na → 2NaNH2 + H2
Câu 10: Muối được làm bột nở trong thực phẩm là
- (NH4)2CO3.
- Na2CO3.
- NH4HSO3.
- NH4Cl.
Câu 11. Axit axetic có thể làm quỳ tím chuyển sang màu hồng, tác dụng với bazơ, oxit bazơ, kim loại trước H và với muối, bởi vì trong phân tử có chứa
- nguyên tử O.
- 3 nguyên tử C, H, O.
- nhóm –CH3
- có nhóm –COOH.
Câu 12. Dãy chất tác dụng với axit axetic là
- ZnO; Cu(OH)2; Cu; CuSO4; C2H5OH.
- CuO; Ba(OH)2; Zn ; Na2CO3; C2H5OH.
- Ag; Cu(OH)2; ZnO; H2SO4; C2H5OH.
- H2SO4; Cu(OH)2; C2H5OH; C6H6; CaCO3.
Câu 13. Trong công nghiệp một lượng lớn axit axetic được điều chế bằng cách
- nhiệt phân metan sau đó làm lạnh nhanh.
- lên men dung dịch rượu etylic.
- oxi hóa etan có xúc tác và nhiệt độ thích hợp.
- oxi hóa butan có xúc tác và nhiệt độ thích hợp.
Câu 14. Phản ứng giữa axit axetic với dung dịch bazơ thuộc loại
- phản ứng oxi hóa – khử.
- phản ứng hóa hợp.
- phản ứng phân hủy.
- phản ứng trung hòa.
Câu 15. Để phân biệt dung dịch axit axetic và rượu etylic ta dùng kim loại nào sau đây?
- Na.
- Zn.
- K.
- Cu.
Đáp án
| 1.A | 2.A | 3.A | 4.D | 5.D |
| 6.A | 7.C | 8.D | 9.D | 10.C |
| 11D | 12B | 13D | 14D | 15B |
Từ việc tổng hợp các hợp chất quan trọng, đến ứng dụng trong phân tích hóa học, nghiên cứu y học, phản ứng HCOOH AgNO3 NH3 đóng góp tích cực vào sự phát triển và tiến bộ của khoa học, công nghệ. Cùng tiếp tục nghiên cứu và khám phá thêm về phản ứng này sẽ mở ra những cánh cửa mới và tiềm năng vượt trội trong nhiều lĩnh vực ứng dụng.
Xem thêm: